NEUMOTIDE - Aerosol para inhalación
Sustancia(s):
- Fluticasona, Salmeterol
Presentaciones:
- 1 Envase(s), 120 Dosis, 6/7,2 ml/g
COMPOSICIÓN:
Cada dosis de NEUMOTIDE 125/25 contiene:
Salmeterol base micronizado (como hidroxinaftoato) 25,00 mcg (equivale a 36,325 mcg de salmeterol hidroxinaftoato)
Fluticasona propionato micronizado 125,00 mcg
Cada dosis de NEUMOTIDE 250/25 contiene:
Salmeterol base micronizado (como hidroxinaftoato) 25,00 mcg (equivale a 36,325 mcg de salmeterol hidroxinaftoato)
Fluticasona propionato micronizado 250,00 mcg
Excipientes: ácido oleico, etanol absoluto, propelente HFA 134a
Este medicamento es Libre de Gluten
INDICACIONES TERAPÉUTICAS:
Acción terapéutica:
Acción antiinflamatoria a nivel pulmonar y broncodilatadora de acción prolongada.
Código ATC: R03AK06.
Indicaciones:
NEUMOTIDE aerosol está indicado en el tratamiento regular de la obstrucción respiratoria reversible, incluyendo asma en niños y adultos, en donde el empleo de una combinación de un broncodilatador y de un corticosteroide inhalado es apropiada. Podría incluir:
• Pacientes bajo dosis efectivas de mantenimiento de β-agonistas de larga duración y corticosteroides inhalados.
• Pacientes que presentan síntomas bajo la terapia actual con corticosteroides inhalados.
• Pacientes bajo terapia regular con broncodilatadores que requieren corticosteroides inhalados.
PROPIEDADES FARMACÉUTICAS:
Propiedades farmacológicas:
Acción farmacológica: Estudios clínicos con salmeterol.
Asma:
Un extenso estudio estadounidense (Salmeterol Multi-center Asthma Research Trial, SMART) comparó la seguridad de salmeterol o placebo sumado a la terapia habitual. No existieron diferencias significativas en el criterio de evaluación primario de los números combinados de muertes relacionadas a trastornos respiratorios y experiencias relacionadas con riesgo de vida a causa de trastornos respiratorios. El estudio mostró un aumento significativo en muertes relacionadas a asma en pacientes que recibían salmeterol (13 muertes de 13.176 pacientes tratados por 28 semanas con salmeterol versus 3 muertes de 13.179 pacientes con placebo).
El estudio no fue diseñado para evaluar el impacto del uso concurrente de corticosteroides inhalados. Sin embargo, el análisis post hoc mostró que no existían diferencias significativas entre los grupos de tratamiento para muertes relacionadas a asma para aquellos pacientes que utilizan esteroides inhalados de base (4/6.127 con salmeterol versus 3/6.138 con placebo). El número de muertes relacionadas a asma en los grupos que no utilizaron esteroides inhalados fue de 9/7.049 con salmeterol versus 0/7.041 con placebo. Más aún, un metaanálisis de 42 estudios clínicos que involucraron 8.030 pacientes con salmeterol/propionato de fluticasona y 7.925 pacientes con propionato de fluticasona no mostró una diferencia estadística entre salmeterol/propionato de fluticasona y propionato de fluticasona en cuanto a eventos respiratorios serios relacionados u hospitalizaciones relacionadas a asma.
Eficacia clínica:
Asma:
Un estudio de 12 meses de duración (Gaining Optimal Asthma Control, estudio GOAL), investigó la eficacia y la seguridad de salmeterol/propionato de fluticasona comparado con esteroides inhalatorios solos en 3.416 pacientes asmáticos. Se definieron varios grados del control del asma como parámetros. La dosis se incrementó cada 12 semanas hasta alcanzar el “control total del asma” o alcanzar la máxima dosis posible de la medicación en estudio. Se consideró que un paciente obtuvo un “buen control del asma”* o un “control total del asma”** si los siguientes criterios se alcanzaban por lo menos 7 de 8 semanas consecutivas de tratamiento.
El estudio mostró:
• 71% de los pacientes tratados con salmeterol/propionato de fluticasona alcanzaron un “buen control del asma”, comparado con el 59% de pacientes tratados solamente con esteroides inhalatorios.
• 41% de los pacientes tratados con salmeterol/propionato de fluticasona alcanzaron un “control total del asma”, comparado con el 28% de pacientes tratados solamente con esteroides inhalatorios. “Buen control del asma” y “control total del asma” se observaron antes con salmeterol/propionato de fluticasona que con esteroides inhalatorios solos, y con una dosis menor de corticosteroide.
El estudio GOAL también mostró:
• El índice de exacerbaciones en el grupo tratado con salmeterol/propionato de fluticasona fue un 29% menor comparado con el grupo tratado solamente con corticosteroides inhalatorios.
• El tratamiento con el objetivo “control total del asma” o “buen control del asma”, condujo a una mejoría en la calidad de vida de los pacientes. El 61% de los pacientes informaron poco o ningún deterioro de la calidad de vida, luego del tratamiento con salmeterol/propionato de fluticasona, mientras que esto sólo se aplica al 8% de los pacientes al principio del estudio.
La calidad de vida se determinó por un cuestionario específico para asma.
*”Buen control del asma”: síntomas ocasionales o uso ocasional de medicación de rescate u ocasionalmente un valor de pico flujo por debajo del 80% del predictivo, pero sin despertares nocturnos, sin exacerbaciones y sin efectos adversos que resulten en un cambio de tratamiento.
**”Control total del asma”: ningún síntoma, ningún uso de medicación de rescate, todos los valores de pico flujo por encima del 80% del predictivo, sin despertares nocturnos, sin exacerbaciones y sin efectos adversos que resulten en un cambio de tratamiento.
Dos estudios adicionales demostraron que, comparado con los pacientes que recibieron solamente esteroides inhalados, los pacientes tratados con salmeterol/propionato de fluticasona lograron una mejoría en la función pulmonar, tuvieron más días libres de síntomas de asma y necesitaron menos medicación de rescate, aunque la dosis de corticosteroide fue un 60% menor en el grupo de salmeterol/propionato de fluticasona que en el grupo de comparación.
El control de los parámetros inflamatorios (medidos en biopsias y lavado bronquial) se mantuvo en ambos grupos. Estudios adicionales demostraron que el tratamiento con salmeterol/propionato de fluticasona mejoró significativamente los síntomas de asma, la función pulmonar y redujo significativamente el uso de medicación de rescate, comparado con los componentes individuales o placebo. Los resultados del estudio GOAL demostraron que estas mejorías con salmeterol/propionato de fluticasona pueden mantenerse por lo menos durante 12 meses. salmeterol y propionato de fluticasona, tienen diferentes modos de acción. El salmeterol protege contra los síntomas, mientras que el propionato de fluticasona mejora la función pulmonar y previene las exacerbaciones de la condición. Salmeterol/propionato de fluticasona pueden ofrecer un régimen más conveniente para los pacientes bajo terapia concurrente con β-agonistas y terapia corticosteroidea inhalada.
A continuación se discuten los mecanismos de acción respectivos de cada uno de los fármacos:
Salmeterol:
Salmeterol es un agonista selectivo y de larga duración (12 horas) de los receptores β-adrenérgicos con una larga cadena lateral que se une al exo-sitio del receptor. Estas propiedades farmacológicas del salmeterol ofrecen una mayor protección efectiva contra la broncoconstricción inducida por histamina y una mayor duración de la broncodilatación, que dura al menos 12 horas, que las dosis recomendadas de los β2-agonistas de corta duración convencionales. Las pruebas in vitro han demostrado que salmeterol es un inhibidor poderoso y de larga duración de la liberación en el pulmón humano, de mediadores de los mastocitos como histamina, leucotrienos y prostaglandina D2. En humanos, el salmeterol inhibe la respuesta de fase temprana y tardía al alérgeno inhalado; el último persiste durante más de 30 horas después de una dosis única cuando el efecto broncodilatador ha dejado de ser evidente. La dosificación única con salmeterol atenúa la hiperrespuesta bronquial. Estas propiedades indican que salmeterol presenta una actividad adicional no broncodilatadora, pero no se tiene claro el significado clínico completo.
Este mecanismo es diferente del efecto antiinflamatorio de los corticosteroides.
Propionato de fluticasona:
El propionato de fluticasona administrado por inhalación en las dosis recomendadas posee una acción glucocorticoidea antiinflamatoria en los pulmones, que produce una reducción en los síntomas y exacerbaciones del asma, sin el efecto adverso observado cuando se administran los corticosteroides sistémicamente. Generalmente, el rendimiento diario de las hormonas adrenocorticales permanece dentro de la gama normal durante el tratamiento crónico con propionato de fluticasona inhalado, aún a la dosis más alta recomendada en niños y adultos. Después de la transferencia de otros esteroides inhalados, el rendimiento diario mejora gradualmente a pesar del uso intermitente pasado y presente de esteroides orales, demostrando así el regreso a la función suprarrenal normal con el Propionato de Fluticasona inhalado. La reserva suprarrenal también continúa siendo normal durante el tratamiento crónico, determinada mediante un aumento normal durante una prueba de estímulo. Sin embargo, cualquier trastorno residual de la reserva suprarrenal a causa del tratamiento previo podría persistir durante un tiempo considerable y esto deberá recordarse.
Farmacocinética:
En animales o humanos, no se tiene evidencia de que la administración inhalada conjunta de salmeterol y propionato de fluticasona afecte la farmacocinética de cualquiera de los componentes. Por lo tanto, desde el punto de vista farmacocinético, cada componente puede considerarse separadamente. En un estudio cruzado de interacción de drogas en 15 sujetos sanos, controlado con placebo, la coadministración de salmeterol (50 mcg inhalado dos veces al día) y el inhibidor del CYP3A4 ketoconazol (400 mg una vez al día por vía oral) por 7 días resultó en un aumento significativo de la exposición plasmática de salmeterol (1,4 veces la Cmáx y 15 veces el ABC –área bajo la curva–). No hubo aumento en la acumulación de salmeterol con dosis repetidas. Se discontinuó el tratamiento con salmeterol y ketoconazol administrado concomitantemente en tres sujetos, debido a la prolongación del intervalo QTc o a las palpitaciones con taquicardia sinusal. En los restantes 12 sujetos, la coadministración de salmeterol y ketoconazol no resultó en un efecto clínicamente significativo en el ritmo cardíaco, potasio sanguíneo o duración del intervalo QTc (ver Advertencias y precauciones - Interacciones).
Salmeterol:
El salmeterol actúa localmente en los pulmones, por lo que los niveles plasmáticos no son una indicación de los efectos terapéuticos. Además, sólo se cuenta con datos limitados sobre la farmacocinética de salmeterol debido a las dificultades técnicas de analizar el fármaco en plasma debido a las bajas concentraciones plasmáticas en las dosis terapéuticas (aproximadamente 200 pg/mL o menos) alcanzadas durante la dosificación inhalada. Después de la dosificación regular con hidroxinaftoato de salmeterol, puede detectarse el ácido hidroxinaftoico en la circulación sistémica, alcanzando concentraciones en estado estable de aproximadamente 100 ng/mL. Estas concentraciones llegan a ser 1.000 veces más bajas que los niveles en el estado estable observadas en los estudios de toxicidad. No se han observado efectos perjudiciales después de la dosificación regular a largo plazo (más de 12 meses) en pacientes con obstrucción respiratoria.
Propionato de fluticasona:
La biodisponibilidad absoluta del propionato de fluticasona ha sido estimada para cada dispositivo de inhalación disponible, a partir de la información de estudios farmacocinéticos de la vía endovenosa e inhalada y por comparaciones entre ellos. En sujetos adultos sanos la biodisponibilidad absoluta ha sido estimada para propionato de fluticasona diskus (7,8%), propionato de fluticasona diskhaler (9,0%), propionato de fluticasona aerosol (10,9%), salmeterol/propionato de fluticasona aerosol (5,3%) y salmeterol/propionato de fluticasona diskus (5,5%), respectivamente. La absorción sistémica ocurre principalmente a través de los pulmones y es inicialmente rápida y después prolongada. El resto de la dosis inhalada podría tragarse, pero contribuye mínimamente a la exposición sistémica debido a la baja solubilidad acuosa y metabolismo presistémico, lo que causa una disponibilidad oral de menos del 1%. Existe un aumento lineal en la exposición sistémica al aumentar la dosis inhalada. La eliminación del propionato de fluticasona está caracterizada por un clearance plasmático elevado (1.150 mL/min), un alto volumen de distribución en estado estacionario (aproximadamente 300 L) y una vida media terminal de aproximadamente 8 horas. La unión a las proteínas del plasma es moderadamente alta (91%). El propionato de fluticasona se elimina muy rápidamente de la circulación sistémica, principalmente por metabolismo a un metabolito inactivo del ácido carboxílico, mediante la enzima de citocromo P450, CYP3A4. La eliminación renal del propionato de fluticasona es despreciable (0,2%) y menos del 5% es como el metabolito. Deberá tenerse cuidado al coadministrarse con inhibidores conocidos de CYP3A4, ya que podría aumentarse la exposición sistémica al propionato de fluticasona.
CONTRAINDICACIONES:
NEUMOTIDE está contraindicado en pacientes con historia de hipersensibilidad a cualquiera de sus componentes.
REACCIONES ADVERSAS:
Podrían esperarse el tipo y gravedad de las reacciones adversas asociadas con salmeterol y/o propionato de fluticasona.
No existe incidencia de reacciones adversas adicionales después de la administración concurrente de los dos compuestos.
A continuación se indican las reacciones adversas asociadas con salmeterol/propionato de fluticasona, clasificadas por órganos y frecuencia. Las frecuencias se han definido de la siguiente forma: muy frecuentes (1/10), frecuentes (1/100 a <1/10), poco frecuentes (1/1.000 a < 1/100), raras (1/10.000 a < 1/1.000) y frecuencia no conocida (no puede estimarse a partir de los datos disponibles). Las frecuencias se han identificado a partir de los datos de ensayos clínicos. No se tuvo en cuenta la incidencia en el grupo placebo.
|
Clasificación de órganos según MedDRA |
Reacciones adversas |
Frecuencia |
|
Infecciones e infestaciones |
Candidiasis en la boca y garganta |
Frecuentes |
|
Neumonía, Bronquitis |
Frecuentes1,3 |
|
|
Candidiasis esofágica |
Raras |
|
|
Trastornos del sistema inmunológico |
Reacciones de hipersensibilidad con las siguientes manifestaciones: |
|
|
Reacciones de hipersensibilidad cutánea; Síntomas respiratorios (disnea) |
Poco frecuentes |
|
|
Angioedema (principalmente edema facial y orofaríngeo); Síntomas respiratorios (broncoespasmo); Reacciones anafilácticas incluyendo shock anafiláctico. |
Raras |
|
|
Trastornos endocrinos |
Síndrome de Cushing, aspecto Cushingoide, supresión suprarrenal, retraso en el crecimiento de niños y adolescentes, disminución de la densidad mineral del hueso. |
Rara |
|
Trastornos del metabolismo y de la nutrición |
Hipocalemia |
Frecuentes3 |
|
Hiperglucemia |
Poco frecuentes |
|
|
Trastornos psiquiátricos |
Ansiedad; Trastornos del sueño |
Poco frecuentes |
|
Cambios en el comportamiento, incluidos hiperactividad psicomotora e irritabilidad (predominantemente en niños) |
Raras |
|
|
Depresión, agresividad (predominantemente en niños) |
Frecuencia no conocida |
|
|
Trastornos del sistema nervioso |
Cefalea |
Muy Frecuentes1 |
|
Temblor |
Poco frecuentes |
|
|
Trastornos oculares |
Cataratas |
Poco frecuentes |
|
Glaucoma |
Raras |
|
|
Visión borrosa |
No conocida |
|
|
Trastornos cardiacos |
Palpitaciones; Taquicardia |
Poco frecuentes |
|
Arritmias cardíacas (incluyendo, taquicardia supraventricular y extrasístoles) |
Raras |
|
|
Fibrilación auricular, Angina de pecho |
Poco frecuentes |
|
|
Trastornos respiratorios, torácicos y mediastínicos |
Nasofaringitis |
Muy Frecuentes2,3 |
|
Irritación de garganta; Ronquera/disfonía |
Frecuentes |
|
|
Sinusitis |
Frecuentes1,3 |
|
|
Broncoespasmo paradójico |
Raras |
|
|
Trastornos de la piel y del tejido subcutáneo |
Contusiones |
Frecuentes1,3 |
|
Trastornos musculoesqueléticos y del tejido conjuntivo |
Calambres musculares; Artralgia; Mialgia |
Frecuentes |
|
Fracturas traumáticas |
Frecuentes1,3 |
1 Notificado frecuentemente con placebo
2 Notificado muy frecuentemente con placebo
3 Notificado durante un estudio de EPOC de 3 años
Pruebas clínicas con salmeterol/propionato de fluticasona: Ha habido informes poco comunes de contusiones. Se han reportado comúnmente los siguientes efectos indeseables: ronquera/disfonía, irritación de la garganta, dolor de cabeza, candidiasis en la boca y garganta y palpitaciones. Neumonía (en pacientes que padecen EPOC).
Etapa postcomercialización con salmeterol/propionato de fluticasona:
Se han reportado, en forma poco común, reacciones de hipersensibilidad cutánea. Raramente, ha habido también reportes de reacciones de hipersensibilidad que se han manifestado como angioedema (principalmente facial y edema orofaríngeo), síntomas respiratorios (disnea y/o broncoespasmo) y muy raramente, reacciones anafilácticas. Muy raramente se ha reportado ansiedad, trastornos del sueño y cambios en el comportamiento, incluyendo hiperactividad e irritabilidad (predominantemente en niños). También se ha reportado muy raramente hiperglucemia.
PRECAUCIONES Y ADVERTENCIAS:
Normalmente, el control de la obstrucción respiratoria reversible deberá seguir un programa escalonado, deberá observarse la respuesta del paciente clínicamente y mediante pruebas de la función pulmonar. Salmeterol/propionato de fluticasona aerosol no es para el alivio de los síntomas agudos cuando se requiere un broncodilatador rápido y de corta duración (por ej.: salbutamol). Se deberá aconsejar a los pacientes que tengan a mano su medicamento de rescate en todo momento. El aumento en el uso de los broncodilatadores de corta duración para aliviar los síntomas del asma indica un deterioro en el control del asma. El deterioro súbito y progresivo en el control del asma podría poner en peligro la vida y el paciente deberá ser evaluado por un médico. Se deberá considerar el aumento en la terapia corticosteroidea. Además, cuando la dosis de salmeterol/propionato de fluticasona no controle adecuadamente la obstrucción respiratoria reversible, el paciente deberá ser revisado por el médico.
Deberán considerarse terapias corticosteroideas adicionales, e incluir la administración de antibióticos si presenta infección. El tratamiento con salmeterol/propionato de fluticasona no deberá suspenderse abruptamente. Hubo un incremento en el reporte de neumonía en estudios de pacientes con EPOC que recibían salmeterol/propionato de fluticasona (ver Reacciones adversas). Los médicos deben estar en alerta del posible desarrollo de neumonía en pacientes con EPOC ya que las características clínicas de la neumonía y la exacerbación frecuentemente se superponen.
Como con todos los medicamentos inhalados que contienen corticosteroides, deberá administrarse salmeterol/propionato de fluticasona con precaución en aquellos pacientes con tuberculosis activa o inactiva. salmeterol/propionato de fluticasona deberá administrarse con precaución en pacientes con tirotoxicosis. Efectos cardiovasculares, como incrementos de la presión sanguínea sistólica y de la frecuencia cardíaca, pueden ocasionalmente ser observados con todas las drogas simpaticomiméticas, especialmente a dosis mayores terapéuticas. Por esta razón, salmeterol/propionato de fluticasona debe ser usado con precaución en pacientes con enfermedad cardiovascular pre-existente. Puede ocurrir una disminución del potasio sanguíneo con todas las drogas simpaticomiméticas, a dosis mayores que las terapéuticas. Por lo tanto, salmeterol/propionato de fluticasona debe ser usado con precaución en pacientes con predisposición a tener niveles bajos de potasio sanguíneo.
Los efectos sistémicos podrían ocurrir con cualquier corticosteroide inhalado, especialmente cuando se usan dosis altas durante períodos largos; estos efectos son mucho menos probables que con los corticosteroides orales. Entre los posibles efectos sistémicos están: síndrome de Cushing, características de tipo Cushing, supresión suprarrenal, retardo en el crecimiento infantil y adolescente, disminución en la densidad mineral ósea, cataratas y glaucoma. Por lo tanto, es importante que se titule la dosis del corticosteroide inhalado a la menor dosis en la que se mantiene un control efectivo. La posibilidad de un deterioro en la respuesta adrenal debería ser siempre tenida en cuenta en aquellas situaciones tanto de emergencia como programadas que puedan producir stress y, en dichos casos, debería ser considerado un tratamiento corticosteroide apropiado (ver Sobredosificación). Se recomienda que se revise regularmente la altura de los niños que reciban tratamiento prolongado con corticosteroides inhalados.
Algunas personas podrían mostrar una mayor susceptibilidad a los efectos de los corticosteroides inhalados que la mayoría de los pacientes. Debido a la posibilidad de trastornos en la respuesta suprarrenal, los pacientes que se transfieren de la terapia con esteroides orales a la terapia con propionato de fluticasona inhalado deberán ser tratados con especial cuidado, y deberá verificarse regularmente la función adrenocortical. Después de la introducción del propionato de fluticasona inhalado, se deberá eliminar la terapia sistémica gradualmente y se deberá alentar a los pacientes a llevar una tarjeta de aviso de esteroides en donde se indique que en épocas de tensión podría ser necesario el uso de terapia adicional. En contadas ocasiones, la terapia inhalada podría enmascarar las condiciones eosinofílicas subyacentes (por ej.: síndrome de Churg y Strauss).
Normalmente, estos casos han estado asociados con la reducción o eliminación de la terapia corticosteroidea oral. No se ha establecido una relación causal directa. Se han reportado muy raramente incrementos en los niveles de la glucosa plasmática (ver Reacciones adversas) y debería ser considerado cuando se prescribe a pacientes con antecedentes de diabetes mellitus. Durante el uso poscomercialización, se han reportado interacciones clínicamente significativas en pacientes que recibieron propionato de fluticasona y ritonavir, resultando en efectos corticosteroideos sistémicos, incluyendo síndrome de Cushing y supresión adrenal. Debido a lo anteriormente mencionado, debe evitarse el uso concomitante del propionato de fluticasona y ritonavir, a menos que el potencial beneficio para el paciente sea mayor que el riesgo de los efectos corticosteroideos sistémicos. (ver Interacciones). La información proveniente del extenso estudio estadounidense (SMART) que compara la seguridad de salmeterol (un componente de NEUMOTIDE) o placebo sumado a la terapia habitual mostró un aumento significativo de muertes relacionadas a asma en pacientes que recibieron salmeterol. La información de este estudio sugiere que los pacientes afro-americanos pueden estar en mayor riesgo de eventos respiratorios serios relacionados o de muerte cuando utilizan salmeterol comparado con placebo.
Se desconoce si esto se debe a la farmacogenética o a otros factores. El estudio SMART no fue diseñado para determinar si el uso concurrente de corticosteroides inhalados modifica el riesgo de muerte relacionada a asma (ver Estudios clínicos con salmeterol). En un estudio de interacción de drogas se observó que el uso concomitante de ketoconazol sistémico aumenta la exposición a salmeterol. Esto puede conducir a la prolongación del intervalo QTc. Debe tenerse precaución cuando inhibidores potentes del CYP3A4 (por ej.: ketoconazol) se coadministran con salmeterol (ver Interacciones y Farmacocinética).
Interacciones:
Los β-bloqueantes selectivos y no selectivos deberán evitarse en aquellos pacientes con obstrucción respiratoria reversible, a menos que se tengan razones imperiosas para usarlos. En circunstancias normales, luego de la administración inhalatoria, se alcanzan concentraciones muy bajas de propionato de fluticasona, debido al mayoritario metabolismo de primer paso y al elevado clearance sistémico mediado por el citocromo P450 3A4 en el intestino e hígado. Debido a esto, es poco probable que se produzcan interacciones con significancia clínica mediadas por el propionato de fluticasona. Un estudio de interacción de la droga en sujetos sanos ha mostrado que el ritonavir (altamente potente inhibidor del citocromo P450 3A4) puede incrementar las concentraciones plasmáticas del propionato de fluticasona, resultando en una marcada reducción de las concentraciones séricas de cortisol. Durante el uso postcomercialización, se han reportado interacciones clínicamente significativas en pacientes que recibieron Propionato de Fluticasona de forma intranasal o inhalada y ritonavir, resultando en efectos corticosteroideos sistémicos, incluyendo síndrome de Cushing y supresión adrenal.
Debido a lo anteriormente mencionado, debe evitarse el uso concomitante del propionato de fluticasona y ritonavir, a menos que el potencial beneficio para el paciente sea mayor que el riesgo de los efectos corticosteroideos sistémicos. Estudios han demostrado que otros inhibidores del citocromo P450 3A4 producen de manera insignificante (eritromicina) y leve (ketoconazol) incrementos en la exposición sistémica al propionato de fluticasona sin reducciones notables en las concentraciones séricas de cortisol. Sin embargo, es aconsejable tener precaución cuando se administra conjuntamente inhibidores potentes del citocromo P450 3A4 (por ej.: ketoconazol), debido al posible incremento de la exposición sistémica al propionato de fluticasona. La coadministración de ketoconazol y salmeterol resultó en un aumento en la exposición del salmeterol plasmático (1,4 veces la Cmáx y 15 veces el ABC) y esto puede producir una prolongación del intervalo QTc (ver Precauciones y advertencias y Farmacocinética).
Embarazo:
Sólo deberá considerarse la administración de fármacos durante el embarazo si los beneficios esperados para la madre son mayores que los riesgos posibles para el feto. No se tiene la suficiente experiencia en el empleo de hidroxinaftoato de salmeterol y propionato de fluticasona durante el embarazo en humanos. Los estudios de toxicidad en la reproducción en animales, ya sea con un fármaco o en combinación, revelaron los efectos sobre el feto que se esperarían con niveles excesivos de exposición sistémica a un agonista de los receptores -adrenérgicos y a un glucocorticosteroide.
Lactancia:
Sólo deberá considerarse la administración de fármacos durante la lactancia si los beneficios esperados para la madre son mayores que los riesgos posibles para el niño. No se tiene la suficiente experiencia en el empleo de hidroxinaftoato de salmeterol y propionato de fluticasona durante la lactancia en humanos. Las concentraciones plasmáticas de salmeterol y propionato de fluticasona después de dosis terapéuticas inhaladas son muy bajas y por lo tanto, es probable que las concentraciones en leche materna humana sean correspondientemente bajas.
Esto está apoyado por estudios en animales durante la lactancia, donde se midieron concentraciones bajas del fármaco en la leche.
No se tienen datos en la leche materna humana.
DOSIS Y VÍA DE ADMINISTRACIÓN:
Posología y forma de administración:
NEUMOTIDE aerosol es sólo para inhalación oral. Se deberá informar a los pacientes que NEUMOTIDE aerosol deberá usarse regularmente para obtener los beneficios óptimos, aun cuando no se presenten síntomas. Un médico deberá reevaluar regularmente a los pacientes, de forma que la acción de NEUMOTIDE continúe siendo la óptima y sólo se modifique bajo orientación médica. La dosis deberá titularse de manera que se use la dosis mínima con la que se mantenga el control efectivo de los síntomas. Donde el control de los síntomas es mantenido con NEUMOTIDE dos veces por día, la titulación a la dosis efectiva más baja podría incluir una inhalación diaria de NEUMOTIDE. Los pacientes deberán recibir la formulación de NEUMOTIDE que contiene la dosis apropiada de propionato de fluticasona para el grado de severidad de la enfermedad. Si el asma está insuficientemente controlado con corticosteroides inhalatorios en monoterapia, el cambio de tratamiento a NEUMOTIDE en dosis terapéuticamente equivalentes a las dosis de corticosteroide, puede conducir a una mejoría en el control del asma. Para pacientes en los cuales el asma está bien controlado con corticosteroides inhalatorios, el cambio de tratamiento a NEUMOTIDE posibilita la reducción de la dosis del corticosteroide mientras se mantiene el mismo control del asma.
Dosis recomendadas:
Adultos y adolescentes desde 12 años:
Dos inhalaciones de 25 mcg de salmeterol (equivale a 36,325 mcg de salmeterol hidroxinaftoato) y 50 mcg de propionato de fluticasona dos veces al día, o dos inhalaciones de 25 mcg de salmeterol y 125 mcg de propionato de fluticasona dos veces al día, o dos inhalaciones de 25 mcg de salmeterol y 250 mcg de propionato de fluticasona dos veces al día.
Niños a partir de 4 años:
Dos inhalaciones de 25 mcg de salmeterol (equivale a 36,325 mcg de salmeterol hidroxinaftoato)y 50 mcg de propionato de fluticasona dos veces al día. No se tienen datos sobre el empleo de NEUMOTIDE en niños menores de 4 años.
Grupos de pacientes especiales:
No es necesario ajustar la dosis en ancianos o en aquellos con trastornos renales o hepáticos.
Instrucciones de uso del aerosol:
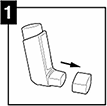
1. Retire la tapa protectora del extremo bucal presionando suavemente de ambos lados de la misma. Verifique que el interior y exterior del extremo bucal esté limpio y no contenga objetos extraños. Ver figura 1.
2. Agite enérgicamente el inhalador para asegurar que cualquier objeto suelto sea removido y que el contenido del aerosol sea mezclado uniformemente.
3. Mantenga el inhalador en posición vertical con el pulgar en la base, por debajo del extremo bucal.
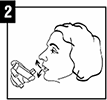
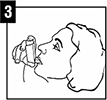
4. Exhale lo más profundo posible, luego rodee el extremo bucal firmemente con los labios, pero sin morderlo. Ver figura 2 y 3.
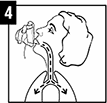
5. Durante la inspiración por la boca, presione con fuerza el inhalador en la parte superior para liberar la dosis y simultaneamente continúe inspirando de modo lento y regular. Ver figura 4.
6. Mientras mantiene la respiración, retire el extremo bucal de su boca y deje de presionar en la parte superior del inhalador. Continúe manteniendo la respiración el mayor tiempo posible y luego espire lentamente por la nariz. Ver figura 5.
7. Si usted va a hacer una segunda inhalación, mantenga el inhalador en posición vertical y espere aproximadamente medio minuto hasta repetir los pasos 2º a 6º. Coloque nuevamente con presión firme la tapa protectora sobre el extremo bucal, y empuje hasta la posición de cierre.
Atención:
No se apure en los pasos 4º, 5º y 6º. Es importante que comience a inspirar del modo más lento posible, justo antes de disparar el aerosol. Practique las primeras aplicaciones frente a un espejo. En caso de observar una “neblina” que se escapa por la parte superior del aerosol o lateralmente de su boca, debería comenzar de nuevo a partir del 2º paso. Si su médico le ha proporcionado instrucciones para el uso del aerosol que dieran de estas, las debe cumplir cuidadosamente. Debe informar a su médico, si no existe claridad al respecto.
Limpieza:
El envase de plástico debe mantenerse limpio. Practique esta limpieza 2 o 3 veces por semana o todos los días.
|
1. Retire la tapa protectora del extremo bucal. |
|
|
2. Remueva el envase metálico del envase plástico. |
|
|
3. Lave el interior del envase plástico colocándolo bajo un chorro de agua potable tanto desde la parte superior como desde la parte inferior. |
|
|
4. Seque el envase de plástico cuidadosamente sacudiéndolo o de ser posible con aire caliente. |
|
|
5. Coloque nuevamente la tapa protectora en el extremo bucal. |
|
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL:
Sobredosificación: La información disponible referente a la sobredosificación con salmeterol y/o propionato de fluticasona se detallan a continuación: los síntomas y signos esperados por sobredosis con salmeterol son aquellos típicos del exceso de estimulación β2-adrenérgica, incluyendo temblor, dolor de cabeza, taquicardia, incremento de la presión sanguínea sistólica e hipokalemia. Los antídotos preferidos son agentes cardioselectivos β-bloqueantes, que deberán usarse con precaución en pacientes con historia de broncoespasmo. Si se tiene que suspender la terapia con salmeterol/propionato de fluticasona debido a una sobredosis del componente β-agonista del fármaco, deberá considerarse el establecimiento de una terapia de reemplazo corticosteroide apropiada. La inhalación aguda del propionato de fluticasona a dosis mayores que las aprobadas pueden conducir a la supresión transitoria del eje hipotalámico-pituitario-adrenal.
Usualmente, esto no requiere una acción de emergencia ya que la función adrenal normal se recupera usualmente dentro de los pocos días. Si se utilizan dosis de salmeterol/propionato de fluticasona mayores a las aprobadas durante períodos prolongados, puede presentarse posiblemente una significativa supresión adrenocortical. Ha habido, muy raramente, reportes de crisis de insuficiencia adrenal aguda, principalmente ocurridas en niños expuestos a dosis mayores a las aprobadas por períodos prolongados (varios meses o años); algunas características observadas han incluido hipoglucemia asociada con disminución de la conciencia y/o convulsiones.
Situaciones que podrían potencialmente desencadenar una crisis de insuficiencia adrenal aguda incluyen traumatismos, intervenciones quirúrgicas, infecciones o cualquier reducción rápida en la dosis del componente propionato de fluticasona inhalado.
No se recomienda que los pacientes reciban dosis de salmeterol/propionato de fluticasona mayores a las aprobadas. Es importante revisar el tratamiento en forma regular y titular en forma descendente hasta la dosis aprobada más baja a la cual se mantiene el control efectivo de la enfermedad (ver Posología y forma de administración).
PRESENTACIÓN:
NEUMOTIDE aerosol se presenta en envases por 120 dosis (6 mL/ 7,2 g).
RECOMENDACIONES SOBRE ALMACENAMIENTO:
Conservación:
No exponer a temperaturas mayores de 50 °C ni a la luz solar. No arrojar al incinerador o al fuego.
No perforar. Prohibido su rellenado. Conservar en su envase original, a temperatura no mayor de 30 °C.
No refrigerar ni congelar.
LEYENDAS DE PROTECCIÓN:
MANTENER ÉSTE Y TODOS LOS MEDICAMENTOS FUERA DEL ALCANCE DE LOS NIÑOS.
Para mayor información y/o reportes de farmaco vigilancia, comunicarse con: farmacovigilancia@berkanafarma.com
E.M.A.M.S. Certificado Nº 49.210.
Elaborado por:
Laboratorio Elea Phoenix S.A.,
Av. Gral. Lemos N° 2809,
Los Polvorines, Pcia. de Buenos Aires, Argentina.
Importado y distribuido por:
BERKANAFARMA S.A.,
Quito - Ecuador.