RISTONEL 50/100/200 - Comprimidos recubiertos
Sustancia(s):
- Sacubitril, Valsartán
Presentaciones:
- 1 Envase(s), 30 Comprimidos recubiertos, 50 mg
- 1 Envase(s), 60 Comprimidos recubiertos, 50 mg
- 1 Envase(s), 30 Comprimidos recubiertos, 100 mg
- 1 Envase(s), 60 Comprimidos recubiertos, 100 mg
- 1 Envase(s), 30 Comprimidos recubiertos, 200 mg
- 1 Envase(s), 60 Comprimidos recubiertos, 200 mg
COMPOSICIÓN:
Cada COMPRIMIDO RECUBIERTO de RISTONEL 50 contiene:
Valsartán 26 mg
Cada COMPRIMIDO RECUBIERTO de RISTONEL 100 contiene:
Valsartán 51 mg
Sacubitrilo (como sacubitrilo sódico) 49 mg
Cada COMPRIMIDO RECUBIERTO de RISTONEL 200 contiene:
Valsartán 103 mg
Sacubitrilo (como sacubitrilo sódico) 97 mg
Excipientes: polivinilpirrolidona, lauril sulfato de sodio, crospovidona, celulosa microcristalina, dióxido de silicio coloidal, talco, estearato de magnesio, óxido de hierro rojo, alcohol polivinílico, polietilenglicol, dióxido de titanio
Este medicamento es libre de gluten
Código ATC: C09DX04
INDICACIONES TERAPÉUTICAS:
Acción terapéutica:
Antagonista de la angiotensina II, otras combinaciones.
Indicaciones:
RISTONEL está indicado:
Para reducir el riesgo de muerte cardiovascular y hospitalización por insuficiencia cardíaca en pacientes con insuficiencia cardíaca crónica (clase II a IV de la New York Association) y fracción de eyección reducida.
RISTONEL se administra por lo general en combinación con otros tratamientos para la insuficiencia cardíaca en lugar de un inhibidor de la enzima convertidora de angiotensina (IECA) o de otro bloqueante del receptor de angiotensina II (ARA II).
PROPIEDADES FARMACÉUTICAS:
Propiedades farmacológicas:
Descripción:
RISTONEL es una combinación a dosis fijas en un mismo comprimido recubierto de un fármaco inhibidor de la neprilisina y un bloqueante del receptor de angiotensina II.
Su masa molecular es 957.99 y su fórmula estructural esquemática es:
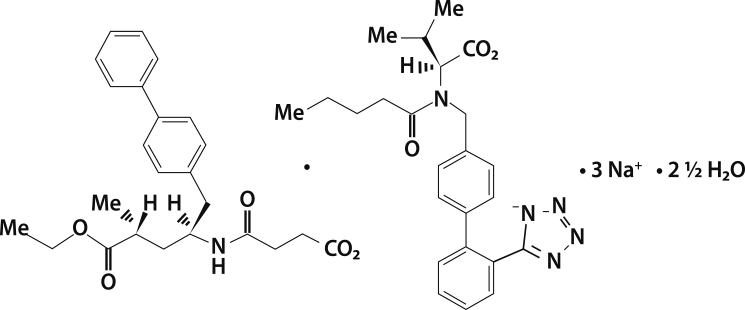
Propiedades farmacodinámicas:
RISTONEL contiene un fármaco inhibidor de la neprilisina, sacubitrilo y un bloqueante del receptor de angiotensina II, valsartán. RISTONEL inhibe la neprilisina que es una endopeptidasa neutra por medio del metabolito activo del profármaco sacubitrilo denominado LBQ657, y bloquea el receptor del tipo 1 de la angiotensina II a través del valsartán.
Los efectos cardiovasculares y renales de RISTONEL en los pacientes que padecen insuficiencia cardíaca se atribuyen a los niveles elevados de péptidos que son degradados por la neprilisina, tales como los péptidos natriuréticos, por LBQ657 y la inhibición en simultáneo de los efectos de la angiotensina II por medio del valsartán. Esta molécula inhibe los efectos de la angiotensina II al bloquear selectivamente el receptor AT1 y también inhibe la liberación de la aldosterona que depende de la angiotensina II.
Se evaluaron los efectos farmacodinámicos de esta combinación (valsartán y sacubitrilo) tras la administración de dosis únicas y repetidas en sujetos sanos y en pacientes con insuficiencia cardíaca, y éstos son consistentes con la inhibición simultánea de neprilisina y el bloqueo del sistema renina angiotensina aldosterona. En un ensayo controlado de 7 días con Valsartán en pacientes con fracción de eyección reducida, la administración de la combinación de valsartán y sacubitrilo dio lugar a un aumento inicial de la natriuresis, aumento de la concentración de GMPc en orina, redujo los niveles plasmáticos del fragmento de la región media del propéptido natriurético auricular y el fragmento aminoterminal del propéptido natriurético auricular de tipo B comparado con valsartán.
En un ensayo de 21 días con pacientes con fracción de eyección reducida la combinación de valsartán y sacubitrilo aumentó significativamente el péptido natriurético auricular, el GMPc en orina y el GMPc en plasma y redujo el propéptido natriurético auricular del tipo B en plasma, aldosterona y endotelina-1 comparado con la situación basal. También se bloqueó el receptor AT1 como se evidencia en el aumento de la actividad de la renina plasmática y las concentraciones plasmáticas de renina. En el ensayo PARADIGM-HF, la combinación de valsartán y sacubitrilo redujo el nivel plasmático del fragmento aminoterminal del propéptido natriurético auricular del tipo B (NT-proBNP) y aumentó el nivel plasmático de péptido natriurético auricular y el de GMPc en orina comparado con enalapril. El BNP no es un biomarcador adecuado para la insuficiencia cardíaca en pacientes tratados con la combinación de sacubitrilo y valsartán debido a que el BNP es un sustrato de la neprilisina. NT-proBNP no es un sustrato de la neprilisina y por ello es un biomarcador más adecuado.
Prolongación del intervalo QTc: En un exhaustivo ensayo clínico de QTc en voluntarios de sexo masculino, sanos, dosis únicas de la combinación de valsartán y sacubitrilo en dosis de hasta 583 mg de sacubitrilo y 617 mg de valsartán no tuvieron efectos en la repolarización cardíaca.
Beta amiloide: La neprilisina es una de las múltiples enzimas involucradas en el aclaramiento β-amiloide (βA) del cerebro y del líquido cefalorraquídeo (LCR). La administración de valsartán y sacubitrilo en dosis de 194 mg y 206 mg, respectivamente una vez al día durante 2 semanas a voluntarios sanos se asoció con un aumento en el LCR de βA1-38 comparado con placebo; no hubo cambios en las concentraciones de βA1-40 y βA 1-42 en el LCR. La relevancia clínica de estos hallazgos se desconoce.
Presión arterial: El agregado de una dosis única de 50 mg de sildenafil a pacientes con concentraciones estables de valsartán y sacubitrilo (en dosis de 194 mg y 206 mg, respectivamente una vez por día durante 5 días) en sujetos con hipertensión arterial se asoció con una reducción adicional de la presión arterial de (5/4 mmHg de presión arterial sistólica y presión arterial diastólica, respectivamente) en comparación con la administración de sólo la combinación de sacubitrilo y valsartán. Tampoco se ve alterada de manera significativa la presión arterial con la administración concomitante de nitroglicerina intravenosa.
Propiedades farmacocinéticas:
Absorción: Luego de la administración oral, la asociación de valsartán y sacubitrilo se disocia en el profármaco sacubitrilo y valsartán. Sacubitrilo posteriormente se metaboliza al metabolito activo LBQ657. Las concentraciones pico de sacubitrilo, LBQ657 y valsartán se alcanzan a las 0.5 horas, 2 horas, y 1.5 horas, respectivamente. La biodisponibilidad oral absoluta de sacubitrilo se estima que es mayor al 60%. valsartán que contiene esta combinación presenta mayor biodisponibilidad que valsartán contenido en otras formulaciones de comprimidos comercializados. El contenido de 26 mg, 51 mg y 103 mg de valsartán de esta combinación es equivalente a 40 mg, 80 mg y 160 mg de valsartán de otras formulaciones en comprimidos que se comercializan.
Tras dos dosis diarias de la combinación sacubitrilo y valsartán, los niveles en estado estacionario de sacubitrilo, LBQ657 y valsartán se alcanzan en tres días. En el estado estacionario, valsartán y sacubitrilo no se acumulan significativamente, mientras que LBQ657 se acumula 1,6 veces. La administración con alimentos no tiene un impacto clínico significativo en la exposición sistémica de sacubitrilo, LBQ657 y valsartán.
RISTONEL se puede administrar con o sin alimentos.
Distribución: Sacubitrilo, LBQ657 y valsartán muestran un alto grado de unión a proteínas plasmáticas (94-97%). De acuerdo con la comparación entre las concentraciones plasmáticas y las del LCR, LBQ657 atraviesa la barrera hematoencefálica en grado limitado (0,28%). El volumen de distribución aparente medio de valsartán y sacubitrilo fue de entre 75 litros y 103 litros, respectivamente.
Metabolismo: Por la acción de esterasas, sacubitrilo se transforma rápidamente en LBQ657, que posteriormente no se metaboliza en una proporción significativa. Valsartán se metaboliza mínimamente, sólo alrededor de un 20% de la dosis se transforma en metabolitos. Se ha identificado en plasma un hidroxilmetabolito de valsartán a concentraciones bajas.
Eliminación: Tras la administración oral, entre un 52 al 68% de sacubitrilo (principalmente como LBQ657) y aproximadamente el 13% de valsartán y sus metabolitos se excretan en orina. Entre el 37 al 48% de sacubitrilo (principalmente como LBQ657) y 86% de valsartán y sus metabolitos se excretan en materia fecal. Sacubitrilo, LBQ657 y valsartán se eliminan en plasma con una vida media de eliminación de aproximadamente 1,43 horas, 11,48 horas y 9,90 horas, respectivamente.
Linealidad/no linealidad: La farmacocinética del sacubitrilo, LBQ657 y valsartán fue lineal en todo el rango de dosis de la combinación sacubitrilo y valsartán.
Grupos especiales:
Pacientes ancianos: La exposición de LBQ657 y valsartán aumentó en los pacientes de más de 65 años en un 42% y 30%, respectivamente cuando se lo compara con sujetos más jóvenes.
Pacientes con insuficiencia renal: Se observó una correlación entre la función renal y la exposición sistémica de LBQ657 en pacientes con insuficiencia renal moderada a grave. La exposición de LBQ657 en pacientes con insuficiencia renal moderada (30 mL/min/1.73 m2 < 60 mL/min/1.73 m2) y grave (15 mL/min/1.73 m2 < 30 ml/min/1.73 m2) fue 1.4 y 2.2 veces superior comparada con pacientes con insuficiencia renal leve (60 mL/min/1.73 m2 < 90 mL/min/1.73 m2). La exposición de valsartán fue similar en pacientes con insuficiencia renal moderada y grave comparada con pacientes con insuficiencia renal leve. No se han llevado a cabo ensayos en pacientes que dializan. Sin embargo, LBQ657 y valsartán se unen en alto grado a proteínas plasmáticos y por ello es improbable que se eliminen de manera efectiva con diálisis.
Pacientes con insuficiencia hepática: En pacientes con insuficiencia hepática de leve a moderada, la exposición a sacubitrilo aumentó en 1,5 y 3,4 veces, LBQ657 aumentó en 1,5 y 1,9 veces y valsartán aumentó en 1,2 y 2,1 veces, respectivamente, comparado con individuos sanos. Sin embargo, en pacientes con insuficiencia hepática leve a moderada, las exposiciones a concentraciones libres de LBQ657 aumentaron en 1,47 y 3,08 veces, respectivamente, y las exposiciones a concentraciones libres de valsartán aumentaron en 1,09 y 2,20 veces respectivamente, comparado con individuos sanos. Esta combinación no se ha estudiado en pacientes con insuficiencia hepática grave, cirrosis biliar o colestasis.
Efectos del sexo: La farmacocinética de la combinación valsartán y sacubitrilo es similar entre hombres y mujeres.
HALLAZGOS DE LABORATORIO CLÍNICO:
Estudios clínicos: Las dosis de 24 mg/ 26 mg, 49 mg/51 mg y 97 mg/ 103 mg de valsartán y sacubitrilo se refirieren en algunas publicaciones como 50, 100 o 200 mg, respectivamente.
El estudio PARADIGM-HF fue un ensayo multinacional, aleatorizado, doble ciego de 8.442 pacientes en el que se comparó la combinación a dosis fijas de valsartán y sacubitrilo con enalapril, ambos administrados a pacientes adultos con insuficiencia cardíaca crónica, clasificación II-IV de NYHA y fracción de eyección reducida (fracción de eyección del ventrículo izquierdo ≤ 40% modificada posteriormente a ≤ 35%) adicionalmente a otro tratamiento para la insuficiencia cardíaca. La variable principal fue la muerte cardiovascular (CV) o la hospitalización por insuficiencia cardíaca (IC). La duración media del seguimiento fue de 27 meses y se trató a los pacientes durante 4,3 años. Se pidió a los pacientes que interrumpieran el tratamiento con inhibidores de la ECA o ARA II y que entraran en un periodo secuencial de preinclusión simple ciego durante el cual recibieron tratamiento con enalapril 10 mg dos veces al día, seguido de un tratamiento ciego con sacubitrilo y valsartán 100 mg dos veces al día, aumentando hasta 200 mg dos veces al día. En ese momento fueron aleatorizados a un periodo doble ciego del ensayo durante el cual recibieron valsartán y sacubitrilo 200 mg o enalapril 10 mg dos veces al día.
La edad media de la población del ensayo fue de 64 años y un 19% tenían 75 años o más. En el momento de la aleatorización, el 70% de los pacientes tenían insuficiencia cardíaca de grado II de la NYHA, 24% de grado III y 0,7% de grado IV. La media de la FEVI fue el 29% y hubo 963 (11,4%) pacientes con una FEVI basal > 35% y ≤ 40%.
En el grupo sacubitrilo y valsartán, un 76% de los pacientes se mantuvieron en la dosis objetivo de 200 mg dos veces al día al final del ensayo (dosis media diaria de 375 mg). En el grupo enalapril, un 75% de los pacientes se mantuvo en la dosis objetivo de 10 mg dos veces al día al final del ensayo (dosis media diaria de 18,9 mg).
La combinación de valsartán y sacubitrilo fue superior frente a enalapril, reduciendo el riesgo de muerte cardiovascular u hospitalización por insuficiencia cardíaca (21,8%) comparado con los pacientes tratados con enalapril (26,5%). La reducción absoluta del riesgo fue de un 4,7% para la combinación de muerte CV u hospitalización por insuficiencia cardíaca, 3,1% para la muerte CV únicamente, y 2,8% para la primera hospitalización por insuficiencia cardíaca únicamente. La reducción relativa del riesgo fue de un 20% frente a enalapril.
Este efecto se observó al inicio y se mantuvo a lo largo de la duración del ensayo. Ambos componentes contribuyeron a la reducción del riesgo. La muerte súbita representó un 45% de muertes cardiovasculares y se redujo en un 20% en los pacientes tratados con valsartán y sacubitrilo comparado con los pacientes tratados con enalapril (HR 0,80, p = 0,0082). Los fallos de bomba representaron un 26% de las muertes cardiovasculares y se redujeron un 21% en los pacientes tratados con valsartán y sacubitrilo comparado con los pacientes tratados con enalapril (HR 0,79, p = 0,0338).
Esta reducción del riesgo se observó de manera consistente en los subgrupos, incluyendo: sexo, edad, raza, geografía, clasificación NYHA (II/III), fracción de eyección, función renal, antecedentes de diabetes o hipertensión, tratamiento previo para la insuficiencia cardíaca y fibrilación auricular. Valsartán y sacubitrilo mejoró la supervivencia con una reducción significativa en la mortalidad de un 2,8% (valsartán y sacubitrilo 17%, enalapril 19,8%). La reducción relativa del riesgo fue del 16% comparado con enalapril.
|
Valsartán y Sacubitrilo |
Enalapril |
Cocientes de riesgos |
Reducción relativa de riesgo |
Valor p |
|
|
Variable principal Punto final compuesto: muerte de causa CV y hospitalización por IC |
914 (21.83%) |
1117 (26.52) |
0.80 (0.73-0.87) |
20% |
0.0000002 |
|
Componentes individuales de la variable principal del punto final compuesto |
|||||
|
Muerte por causas CV |
558 (13.33) |
693 (16.45) |
0.80 (0.71-0.89) |
20% |
0.00004 |
|
Primera hospitalización por IC |
537 (12.83) |
658 (15.62) |
0.79 (0.71-0.89) |
21% |
0.00004 |
|
Variable secundaria |
|||||
|
Muerte por todas las causas |
711 (16.98) |
835 (19.82) |
0.84 (0.76-0.93) |
16 % |
0.00005 |
CONTRAINDICACIONES:
• Hipersensibilidad conocida a los principios activos (sacubitrilo y valsartán) o a los excipientes.
• Pacientes con antecedentes de angioedema relacionado con tratamientos previos con un IECA o ARA II.
• Uso concomitante con IECA. No administrar dentro de las 36 horas posteriores al cambio de un IECA.
• Uso concomitante de aliskiren en pacientes con diabetes o con insuficiencia renal.
• Angioedema hereditario o idiopático.
• Embarazo (sobre todo durante el segundo y tercer trimestre) y lactancia.
EFECTO EN LA CAPACIDAD PARA CONDUCIR Y UTILIZAR MÁQUINAS:
Efectos sobre la capacidad de conducir y operar maquinarias:
La influencia de sacubitrilo y valsartán sobre la capacidad de conducir u operar maquinarias es pequeña. Al conducir u operar maquinarias se debe tener en cuenta que ocasionalmente puede producir mareos o fatiga.
PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD:
Datos de toxicidad preclínica:
Carcinogénesis y mutagénesis:
Los estudios de carcinogénesis conducidos en ratones y ratas con valsartán y sacubitrilo no identificaron ningún potencial carcinogénico para esta combinación. La Cmáx de LBQ657 con la dosis alta de 1200 mg/kg/día en los ratones macho y hembra fue respectivamente de 14 y 16 veces aquella observada en los seres humanos con la máxima dosis recomendada para humanos (MDRH). La Cmáx de LBQ657 en las ratas macho y hembra con dosis de 400 mg/kg/día fue respectivamente de 1.7 y 3.5 veces aquella observada con la MDRH. Las dosis de valsartán estudiadas (dosis altas de 160 y 200 mg/kg/día en ratones y ratas, respectivamente) fueron alrededor de 4 y 10 veces, respectivamente, la MDRH dependiendo de los mg/m2.
Los estudios de mutagenicidad y clastogenicidad conducidos con esta combinación no revelaron ningún efecto a nivel genético y cromosómico.
Deterioro de la fertilidad:
Valsartán y sacubitrilo no demostró ningún efecto sobre la fertilidad en las ratas hasta la dosis de 73 mg de sacubitrilo/77 mg de valsartán /kg/día.
Toxicología animal:
Se evaluaron los efectos de esta combinación sobre las concentraciones de beta amiloide en el LCR y el tejido cerebral en monos cynomolgus jóvenes (de 2 a 4 años) tratados con valsartán y sacubitrilo (24 mg de sacubitrilo/26 mg de valsartán/kg/día) durante dos semanas. En este estudio la combinación valsartán y sacubitrilo afectó la depuración de A beta amiloide del LCR aumentando los niveles de LCR beta amiloide 1-40, 1-42 y 1-38. No hubo aumento correlativo en los niveles de beta amiloide en el cerebro. Además, en el estudio de toxicología conducido en monos con dosis de sacubitrilo 146 mg y valsartán 154 mg/kg/día durante 39 semanas no hubo acumulación de beta amiloide en el cerebro.
REACCIONES ADVERSAS:
Las reacciones adversas notificadas con mayor frecuencia durante el tratamiento con valsartán y sacubitrilo fueron hipotensión, hiperpotasemia e insuficiencia renal. También angioedema.
La seguridad de valsartán y sacubitrilo en pacientes con insuficiencia cardíaca crónica se evaluó en el ensayo pivotal de fase 3 PARADIGM-HF, en el que se compararon pacientes tratados con esta combinación vs enalapril. En este estudio 1.102 pacientes (10,5%) de la rama enalapril discontinuaron de manera permanente el ensayo, 5,6% por una reacción adversa; las más frecuentes fueron insuficiencia renal (1,7%), hiperpotasemia (1,7%) e hipotensión (1,4%). En la rama valsartán y sacubitrilo 10,4% de los pacientes discontinuó de manera permanente, 5,9% por una reacción adversa; las más frecuentes fueron insuficiencia renal (1,8%), hipotensión (1,7%) e hiperpotasemia (1,3%). La interrupción del tratamiento debido a una reacción adversa en el ensayo PARADIGM-HF ocurrió en 450 pacientes tratados con valsartán y sacubitrilo (10,7%) y en 516 pacientes tratados con enalapril (12,2%).
Tabla de reacciones adversas:
Las reacciones adversas se clasifican de acuerdo con el Sistema de Clasificación de Órganos y por intervalos de frecuencia con las más frecuentes en primer lugar utilizando la siguiente convención: muy frecuentes (≥ 1/10); frecuentes (≥ 1/100 a < 1/10); poco frecuente (> 1/1.000 a < 1/100); raras (> 1/10.000 a < 1/1.000); muy raras (< 1/10.000). Dentro de cada intervalo de frecuencia, las reacciones adversas se enumeran en orden decreciente de gravedad.
|
Sistema de clasificación |
Problema |
Frecuencia |
|---|---|---|
|
Transtornos de la sangre y del sistema linfático |
Anemia |
Frecuente |
|
Transtornos del sistema inmunológico Transtornos del metabolismo y de la nutrición |
Hipersensibilidad Hiperpotasemia Hipopotasemia Hipoglucemia |
Poco frecuente Muy frecuente Frecuente Frecuente |
|
Transtornos del sistema nervioso |
Mareo Cefalea Síncope Mareo postural |
Frecuente Frecuente Frecuente Poco frecuente |
|
Transtornos del oído y del laberinto |
Vértigo |
Frecuente |
|
Transtornos vasculares |
Hipotensión Hipotensión ortostática |
Muy frecuente Frecuente |
|
Transtornos respiratorios y mediastínicos |
Tos |
Frecuente |
|
Transtornos gastrointestinales |
Diarrea Náuseas Gastritis Angioedema intestinal |
Frecuente Frecuente Frecuente Muy rara |
|
Transtornos de la piel y del tejido subcutáneo |
Prurito Rash Angioedema |
Poco frecuente Poco frecuente Poco frecuente |
|
Transtornos renales y urinarios |
Insuficiencia renal Insuficiencia renal aguda |
Muy frecuente Frecuente |
|
Transtornos generales |
Fatiga Astenia |
Frecuente Frecuente |
Descripción de reacciones adversas seleccionadas:
Angioedema: Se ha notificado angioedema en pacientes tratados con sacubitrilo y valsartán. En PARADIGM-HF se notificó angioedema en un 0,5% de los pacientes tratados con esta combinación, comparado con un 0,2% de los pacientes tratados con enalapril. Se observó una mayor incidencia de angioedema en pacientes de raza negra tratados con valsartán y sacubitrilo (2,4%) y enalapril (0,5%).
Hiperpotasemia y potasio sérico: En PARADIGM-HF se notificaron hiperpotasemia y concentraciones de potasio sérico > 5,4 mmol/L en 11,6% y 19,7% de los pacientes tratados con valsartán y sacubitrilo y 14,0% y 21,1% de los pacientes tratados con enalapril, respectivamente.
Hemoglobina y hematocrito: Se observaron disminuciones en la hemoglobina/hematocrito de más del 20% en aproximadamente el 5% de los pacientes tratados con valsartán y sacubitrilo como con enalapril en el ensayo clínico doble ciego.
Creatinina: Se observaron incrementos de la creatinina sérica mayores al 50% en el 16% de los pacientes tratados tanto con valsartán y sacubitrilo como con enalapril.
Presión arterial: En PARADIGM-HF se notificaron hipotensión y baja presión arterial sistólica clínicamente relevante (20 mmHg) en un 17,6% y 4,76% de los pacientes tratados con valsartán y sacubitrilo comparado con un 11,9% y 2,67% de los pacientes tratados con enalapril, respectivamente.
Insuficiencia renal: En PARADIGM-HF se notificó insuficiencia renal en un 10.1% de los pacientes tratados con valsartán y sacubitrilo y en un 11,5% de los pacientes tratados con enalapril.
Información para los profesionales de la salud:
Es importante notificar sospechas de efectos adversos al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales de la salud a notificar las sospechas de reacciones adversas al Departamento de Farmacovigilancia del Laboratorio.
RISTONEL cuenta con un Plan de Gestión de Riesgos cuya finalidad es garantizar la seguridad y protección de los pacientes promoviendo el uso correcto del medicamento de acuerdo con las recomendaciones aprobadas y validadas internacionalmente.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO:
Interacciones medicamentosas:
Interacciones que resultan en contraindicaciones:
IECA: el uso concomitante de valsartán y sacubitrilo con medicamentos del grupo de los IECA está contraindicado dado que la inhibición concomitante de neprilisina y de la ECA puede aumentar el riesgo de angioedema.
RISTONEL no se debe iniciar hasta 36 horas después de la última dosis del tratamiento con IECA. El tratamiento con IECA no se debe iniciar hasta 36 horas después de la última dosis de RISTONEL.
Aliskiren: El uso concomitante de valsartán y sacubitrilo con medicamentos que contienen aliskiren está contraindicado en pacientes con diabetes o con insuficiencia renal (< 60 mL/min/1.73 m2). No se recomienda esta combinación con inhibidores directos de la renina como el aliskiren. La combinación de valsartán y sacubitrilo con aliskiren está potencialmente asociada con un aumento de la frecuencia de efectos adversos como hipotensión, hiperpotasemia y disminución de la función renal.
Interacciones que resultan en la no recomendación de uso asociado:
RISTONEL contiene valsartán y por lo tanto no se debe administrar junto con otro medicamento que contenga un ARA II.
Interacciones que requieren precaución:
Sustratos de OATP1B1 y OATP1B3 (estatinas): Los datos in vitro indican que sacubitrilo inhibe los transportadores de OATP1B1 y OATP1B3. RISTONEL puede, por lo tanto, aumentar la exposición sistémica de sustratos de OATP1B1 y OATP1B3 como las estatinas. La administración de valsartán y sacubitrilo aumentó la Cmáx de atorvastatina y sus metabolitos en hasta dos veces y el ABC en hasta 1,3 veces. Se debe tener precaución cuando se administre RISTONEL junto con estatinas. No se observó ninguna interacción medicamentosa clínicamente relevante cuando se administró de forma conjunta con simvastatina.
Inhibidores de la fosfodiesterasa 5 (sildenafil): La adición de una dosis única de sildenafil a valsartán y sacubitrilo en estado estacionario en pacientes con hipertensión se asoció con una reducción significativamente mayor de la presión arterial comparado con la administración de valsartán y sacubitrilo solo. Por ello, se debe tener precaución cuando se inicie sildenafil u otro inhibidor de la PDE-5 en pacientes tratados con RISTONEL.
Medicamentos o sales que modifican el potasio: Al igual que otros fármacos que bloquean la acción de la angiotensina II, el uso concomitante de diuréticos ahorradores de potasio como la espironolactona o el amiloride, suplementos de potasio, sustitutos de la sal (que contiene potasio) pueden producir incrementos del potasio sérico.
Fármacos antiinflamatorios no esteroides (AINEs), incluyendo inhibidores selectivos de la ciclooxigenasa 2 (COX 2): En los adultos mayores, sobre todo los que tienen la función renal comprometida o con depleción de volumen (por ejemplo, aquellos en tratamiento con diuréticos), el uso concomitante de AINEs con RISTONEL puede resultar en un empeoramiento de la función renal, incluso insuficiencia renal aguda. Estos efectos son generalmente reversibles. Se debe monitorear la función renal en forma periódica.
Litio: Se han informado incrementos en las concentraciones séricas de litio y toxicidad por litio durante la administración concomitante de litio con antagonistas del receptor de la angiotensina II. Se debe monitorear los niveles de litio séricos durante el uso concomitante con RISTONEL.
Furosemida: La administración concomitante de RISTONEL con furosemida no tuvo efecto en la farmacocinética de RISTONEL, pero redujo la Cmáx y la ABC de furosemida en un 50% y en un 28%, respectivamente. Mientras que no hubo cambios relevantes en el volumen urinario, la excreción urinaria de sodio se redujo en las 4 horas y 24 horas después de la coadministración.
Nitratos: No hubo interacciones medicamentosas entre RISTONEL y la nitroglicerina intravenosa en relación con la reducción de la presión sanguínea. La administración concomitante de nitroglicerina y RISTONEL se asoció con una diferencia de tratamiento de 5 latidos por minuto en el ritmo cardíaco comparado con la administración de sólo nitroglicerina. Puede ocurrir un efecto similar en la frecuencia cardíaca cuando se coadministra con nitratos vía sublingual, oral o mediante parches transdérmicos. En general, no se requiere ajuste de dosis.
Transportadores OATP y MRP2: Los metabolitos activos de sacubitrilo (LBQ657) y valsartán son sustratos de OATP1B1, OATP1B3, OAT1 y OAT3; valsartán es también un sustrato de MRP2. Por lo tanto, la administración de valsartán y sacubitrilo junto con inhibidores de OATP1B1, OATP1B3, OAT3 (p. ej.: rifampicina, ciclosporina), OAT1 (ej. tenofovir, cidofovir) o de MRP2 (p. ej.: ritonavir) puede aumentar la exposición sistémica de LBQ657 o de valsartán. Se debe tener especial precaución cuando se inicie o se finalice el tratamiento concomitante con dichos medicamentos.
Metformina: La administración concomitante de RISTONEL y metformina redujo tanto la Cmáx como el ABC de metformina en un 23%. No se conoce la relevancia clínica de estos hallazgos. Por lo tanto, cuando se inicie el tratamiento con RISTONEL en pacientes que estén tomando metformina, se debe evaluar el estado clínico del paciente.
Efecto de los fármacos coadministrados con RISTONEL: Dado que el metabolismo de valsartán y sacubitrilo mediado por la enzima CYP450 es mínimo no se espera que la coadministración con fármacos que afectan a las enzimas CYP450 afecte la farmacocinética de esta combinación. Los estudios dedicados a la interacción medicamentosa demostraron que la coadministración de furosemida, warfarina, digoxina, carvedilol, la combinación de levonorgestrel y etinilestradiol, amlodipina, omeprazol, hidroclorotiazida, metformina, atorvastatina y sildenafil no alteró la exposición sistémica a sacubitrilo, LBQ657 ni a valsartán.
PRECAUCIONES Y ADVERTENCIAS:
Advertencias y precauciones:
Consulte a su médico si presenta dolor abdominal, náuseas, vómitos o diarrea después de tomar RISTONEL. Su médico decidirá si continuar con el tratamiento. No deje de tomar RISTONEL por su cuenta.
Bloqueo dual del sistema renina angiotensina aldosterona:
El uso de valsartán y sacubitrilo con un inhibidor de la enzima convertidora de angiotensina está contraindicada debido al aumento de riesgo de angioedema. RISTONEL no se debe iniciar hasta 36 horas después de haber tomado la última dosis del tratamiento con un IECA. Si el tratamiento con RISTONEL se interrumpe, no se debe iniciar el tratamiento con un IECA hasta 36 horas después de la última dosis de RISTONEL.
No se recomienda utilizar la combinación de valsartán y sacubitrilo con fármacos inhibidores directos de la renina como el aliskiren. Está contraindicado en pacientes con diabetes o en pacientes con insuficiencia renal. RISTONEL contiene valsartán. Por ello no se debe administrar junto con otro medicamento que contenga un ARA II.
Hipotensión arterial:
RISTONEL disminuye la presión arterial y puede causar hipotensión sintomática. Los pacientes con un sistema renina angiotensina activado tales como los pacientes con depleción de volumen y/o de sal (como por ejemplo los que toman altas dosis de diuréticos) presentan un mayor riesgo. Se deberá corregir la depleción de volumen o de sal antes de comenzar a tomar RISTONEL o se puede comenzar con una dosis más baja.
Si se produce hipotensión se deberá ajustar la dosis de diuréticos o de los fármacos antihipertensivos que se estén tomando concomitantemente. O tratar las causas de la hipotensión (como por ejemplo la hipovolemia). Si la hipotensión persiste se deberá reducir la dosis de RISTONEL o suspenderlo temporariamente. En general no suele ser necesario interrumpir el tratamiento.
Insuficiencia renal:
La evaluación de pacientes con insuficiencia cardíaca siempre debería incluir una evaluación de la función renal. Los pacientes con insuficiencia renal leve a moderada tienen mayor riesgo de desarrollar hipotensión. La experiencia clínica es muy limitada en pacientes con insuficiencia renal grave (menos de 30 mL/min/1.73 m2); estos pacientes podrían tener un mayor riesgo de hipotensión. No hay experiencia con pacientes en el estadio final de enfermedad renal, por lo cual no se recomienda utilizar este medicamento.
En los pacientes cuya función renal dependa de la actividad del sistema renina angiotensina aldosterona (como por ejemplo los pacientes con insuficiencia cardíaca severa) el tratamiento con IECA y ARA II fue asociado a oliguria, uremia progresiva y rara vez insuficiencia renal aguda y muerte. Se deberá monitorear la creatinina sérica y reducir la dosis o suspender RISTONEL en los pacientes que desarrollan una disminución de la función renal de relevancia clínica.
Al igual que todos los fármacos que afectan el sistema renina angiotensina aldosterona, RISTONEL puede incrementar los niveles de urea y creatinina plasmáticos en pacientes con estenosis renal unilateral y bilateral. En los pacientes con estenosis de la arteria renal se deberá monitorear la función renal.
Hiperpotasemia:
No se debe iniciar el tratamiento si los niveles de potasio sérico son > 5.4 mmol/L. El uso de valsartán y sacubitrilo se puede asociar con un aumento del riesgo de hiperpotasemia, aunque también se podría presentar hipopotasemia. Se recomienda la monitorización de los niveles séricos de potasio, especialmente en pacientes con factores de riesgo como insuficiencia renal, diabetes mellitus o hipoaldosteronismo, o que reciben dietas altas en potasio o en tratamiento con antagonistas de mineralocorticoides. Si los pacientes experimentan hiperpotasemia clínicamente significativa, se recomienda un ajuste de los medicamentos concomitantes o la disminución temporal de la dosis de valsartán y sacubitrilo o su interrupción. Si el nivel de potasio sérico es > 5,4 mmol/L, se debe considerar la interrupción.
Angioedema:
Se ha notificado angioedema en pacientes tratados con sacubitrilo y valsartán. Si se produce angioedema, este medicamento se debe interrumpir inmediatamente y se debe instaurar un tratamiento y una monitorización apropiada hasta la resolución completa y sostenida de los signos y síntomas. No se debe volver a administrar. En los casos de angioedema en los que la hinchazón se limitaba a cara y labios, éste se resolvió sin tratamiento, aunque los antihistamínicos han sido útiles en el alivio de los síntomas. El angioedema asociado con edema de laringe puede ser mortal. Cuando están involucradas la lengua, glotis o la laringe con probabilidad de causar obstrucción de la entrada de aire, se debe administrar rápidamente un tratamiento apropiado, por ej.: solución de adrenalina 1 mg/1 mL (0,3-0,5 mL), y/o las medidas necesarias para garantizar el flujo de entrada de aire. No se han estudiado pacientes con antecedentes previos de angioedema. Dado que podrían tener un riesgo mayor de angioedema, se recomienda precaución si este medicamento se utiliza en estos pacientes. Valsartán y sacubitrilo está contraindicado en pacientes con antecedentes conocidos de angioedema relacionado con un tratamiento anterior con IECA o ARA II o con angioedema hereditario o idiopático. Los pacientes de raza negra tienen una susceptibilidad mayor a desarrollar angioedema.
Angioedema intestinal:
Se han notificado casos de angioedema intestinal en pacientes tratados con antagonistas de los receptores de la angiotensina II, incluyendo valsartán (ver Reacciones adversas). Estos pacientes presentan dolor abdominal, náuseas, vómitos y diarrea. Los síntomas se resolvieron tras la interrupción de los antagonistas de los receptores de la angiotensina II. Si se diagnostica angioedema intestinal, se debe interrumpir el tratamiento con valsartán e iniciar un seguimiento adecuado hasta que se haya producido la resolución completa de los síntomas.
Uso en poblaciones especiales:
Embarazo: No se recomienda el uso de valsartán y sacubitrilo durante el primer trimestre de embarazo y está contraindicado durante el segundo y tercer trimestre de embarazo.
No hay datos en la utilización de valsartán y sacubitrilo en mujeres embarazadas. Los estudios en animales con este medicamento han mostrado toxicidad para la reproducción.
Con valsartán: La evidencia epidemiológica en relación con el riesgo de teratogenicidad tras la exposición a IECA durante el primer trimestre de embarazo no es concluyente; sin embargo, no se puede excluir un pequeño aumento del riesgo. Dado que no hay datos epidemiológicos controlados sobre el riesgo con ARA II, pueden existir riesgos similares para esta clase de medicamentos. A menos que se considere esencial la continuación de la terapia con ARA II, a las pacientes que planifiquen un embarazo se les debe cambiar a tratamientos antihipertensivos alternativos que tengan un perfil de seguridad establecido para su uso en el embarazo. Cuando se conozca el embarazo, se debe interrumpir inmediatamente el tratamiento con ARA II y, si es necesario, se debe iniciar un tratamiento alternativo. Se sabe que la exposición al tratamiento con ARA II durante el segundo y tercer trimestre induce fetotoxicidad humana (disminución de la función renal, oligohidramnios, retraso en la osificación craneal) y toxicidad neonatal (fallo renal, hipotensión, hiperpotasemia). En el caso de que la exposición a ARA II haya tenido lugar a partir del segundo trimestre de embarazo, se recomienda la revisión por ultrasonidos de la función renal y craneal.
Con sacubitrilo: No hay datos de la utilización de sacubitrilo en mujeres embarazadas. Los estudios en animales han mostrado toxicidad para la reproducción. Se deberá observar cercanamente a los neonatos con antecedentes de exposición intrauterina a valsartán y sacubitrilo para detectar la presencia de hipotensión, oliguria e hiperpotasemia. En caso de producida oliguria o hipotensión arterial se deberá evaluar la perfusión renal. Puede ser necesario realizar exsanguinotransfusiones o diálisis como medio para revertir la hipotensión y reemplazar la función renal.
Lactancia: Se desconoce si valsartán y sacubitrilo se excreta en la leche materna. Los componentes de este medicamento, sacubitrilo y valsartán, se excretaron en la leche de ratas lactantes. Debido al potencial riesgo de reacciones adversas en recién nacidos/niños lactantes, no se recomienda durante la lactancia.
Se debe decidir si abstenerse de la lactancia o interrumpir este medicamento durante la lactancia.
Fertilidad: No hay datos disponibles sobre el efecto de valsartán y sacubitrilo en la fertilidad humana. No se han demostrado problemas de fertilidad en los ensayos con ratas macho y hembra.
Pediatría: No se estableció la seguridad y efectividad de RISTONEL en pacientes pediátricos.
Geriatría: No se observaron diferencias farmacocinéticas relevantes en adultos mayores (> 65 años) o muy mayores (> 75 años) en comparación con la población general.
Insuficiencia hepática: No requiere ajuste de dosis cuando se administra este medicamento a pacientes con insuficiencia hepática leve (clasificación A de Child-Pugh). La dosis de inicio para los pacientes con insuficiencia hepática moderada (clasificación B de Child-Pugh) es de 50 mg dos veces por día. No se recomienda usar este medicamento en pacientes con insuficiencia hepática severa (clasificación C de Child-Pugh), debido a que no hay estudios sobre estos pacientes.
Insuficiencia renal: No se requiere ajuste de dosis en insuficiencia renal leve a moderada. En caso de insuficiencia renal severa (< 30 mL/min/1.73 m2) la dosis inicial debería ser de 50 mg dos veces por día.
DOSIS Y VÍA DE ADMINISTRACIÓN:
Posología y forma de administración:
Tratamiento de la insuficiencia cardíaca:
El uso concomitante de RISTONEL con un medicamento inhibidor de la enzima convertidora de angiotensina (IECA) está contraindicado.
Si se cambia un IECA por RISTONEL se deberá dejar transcurrir un período de lavado de 36 horas aproximadamente entre la administración del fármaco anterior (IECA) y el nuevo medicamento (RISTONEL).
La dosis inicial recomendada de RISTONEL es de un comprimido de 100 mg (49 mg/51 mg) dos veces al día.
La dosis se debe duplicar luego de 2 a 4 semanas hasta alcanzar la dosis objetivo de un comprimido de RISTONEL 200 mg (97 mg/103 mg) dos veces al día, en función de la tolerancia del paciente.Se puede tomar con o sin alimentos. Los comprimidos deben ser tragados con un vaso de agua.
Si los pacientes experimentan problemas de tolerancia, como por ejemplo presión arterial sistólica ≤ 95 mmHg, hipotensión sintomática, hiperpotasemia, disfunción renal, entre otras, se recomienda ajustar los medicamentos que se toman en forma concomitante, la reducción temporal de la dosis de RISTONEL o la interrupción de RISTONEL.
Ajuste de la dosis en pacientes que no reciben medicamentos del grupo de los IECA o del grupo de los antagonistas de los receptores de angiotensina II (ARA II) o que reciben dosis bajas de estos fármacos.
La experiencia en pacientes que no estén tomando IECA o ARA II o tomando dosis bajas de estos medicamentos es limitada, por lo tanto, en estos pacientes se recomienda una dosis inicial de 50 mg (24 mg/26 mg) dos veces al día y un aumento lento de dosis (duplicando la dosis cada 2-4 semanas) hasta alcanzar la dosis objetivo de RISTONEL de 200 mg dos veces por día de acuerdo con la tolerancia del paciente.
Grupos especiales:
Pacientes con insuficiencia renal: No se requieren cambios en la posología en caso de pacientes con insuficiencia renal leve a moderada. Se recomienda una dosis de RISTONEL 50 mg (24 mg/26 mg) dos veces por día para los pacientes con insuficiencia renal severa (< 30 mL/min/1.73 m2). Duplicar la dosis de RISTONEL cada 2 a 4 semanas hasta alcanzar la dosis de mantenimiento objetivo de 200 mg (97 mg/103 mg) dos veces al día, de acuerdo con la tolerancia del paciente.
Pacientes con insuficiencia hepática: no se requieren cambios en la posología en caso de pacientes con insuficiencia hepática leve. Se recomienda una dosis de RISTONEL 50 mg (24 mg/26 mg) dos veces por día para los pacientes con insuficiencia hepática moderada (clasificación de Child Pugh B). Duplicar la dosis de RISTONEL cada 2 a 4 semanas hasta alcanzar la dosis de mantenimiento objetivo de 200 mg (97 mg/103 mg) dos veces al día, de acuerdo con la tolerancia del paciente. No se recomienda el uso de este medicamento en pacientes con insuficiencia hepática severa.
Pacientes ancianos: La dosis deberá estar relacionada con la función renal del paciente anciano.
Pacientes pediátricos y adolescentes: No se ha establecido la seguridad y eficacia de esta medicación en menores de 18 años.
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL:
Sobredosis:
Hay información limitada en relación con la sobredosificación en humanos con la combinación de sacubitrilo y valsartán. En los voluntarios sanos se estudiaron las dosis únicas de 583 mg de sacubitrilo y 617 mg de valsartán y las dosis múltiples de 437 mg de sacubitrilo y 463 mg de valsartán durante 14 días. Todas fueron bien toleradas.
La hipotensión es el resultado más probable de la sobredosificación debido a los efectos hipotensores de este medicamento. Se deberá proporcionar tratamiento sintomático. Es improbable que se pueda eliminar valsartán y sacubitrilo mediante diálisis debido a su gran capacidad de unión a proteínas.
Ante la eventualidad de una sobredosificación concurrir al hospital más cercano.
PRESENTACIÓN:
Presentaciones:
RISTONEL 50, 100 y 200 mg: envases conteniendo 30 y 60 comprimidos recubiertos.
Laboratorio Elea Phoenix S.A.,
Av. Gral. Lemos Nº 2809, Los Polvorines,
Pcia. de Buenos Aires, Argentina.
Importado y distribuido por:
BERKANAFARMA S.A.
Quito - Ecuador.
Fecha de última revisión: Marzo/2025.
RISTONEL 50: Reg. San. 8353-MEE-0923
RISTONEL 100: Reg. San. 8358-MEE-0923
RISTONEL 200: Reg. San. 8355-MEE-0923
RECOMENDACIONES SOBRE ALMACENAMIENTO:
Condiciones de conservación y almacenamiento:
Conservar en su envase original, a temperatura no mayor de 30 °C. No utilizar este medicamento después de la fecha de vencimiento. La fecha de vencimiento se encuentra en el embalaje exterior y en cada blíster. La fecha de vencimiento es el último día del mes que se indica.
LEYENDAS DE PROTECCIÓN:
Mantener éste y todos los medicamentos fuera del alcance de los niños. Este medicamento debe ser usado exclusivamente bajo prescripción y vigilancia médica y no puede repetirse sin nueva receta médica.
VENTA BAJO RECETA MÉDICA.
Especialidad Medicinal Autorizada por el Ministerio de Salud. Certificado Nº 59.408.
Para mayor información y/o reportes de Farmacovigilancia, comunicarse con:
farmacovigilancia@berkanafarma.com
