ZALUTEX - Cápsulas duras
Sustancia(s):
- Enzalutamida
Presentaciones:
- 1 Bolsa, 120 Cápsulas duras,
COMPOSICIÓN:
Estructura y Nombre Químico del Principio Activo:
El ingrediente farmacéutico activo utilizado es Enzalutamida de origen sintético. Su nombre químico es: 4-{3-[4-ciano-3-(trifluorometil)fenil]-5,5-dimetil-4-oxo-2-sulfanilideneimidazolidin-1-il}-2-fluoro-N-metilbenzamida.
Estructura Química:
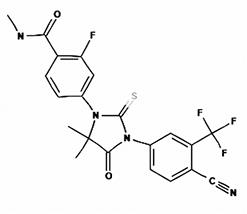
Fórmula Química: C21H16F4N4O2S
INDICACIONES TERAPÉUTICAS:
Indicaciones:
ZALUTEX se encuentra indicado para:
• el tratamiento de hombres adultos con cáncer de próstata resistente a la castración
PROPIEDADES FARMACÉUTICAS:
Farmacologia clinica:
Farmacodinamia:
Mecanismo de acción: Enzalutamida inhibe los receptores de andrógenos actuando sobre diferentes etapas de la vía de señalización. Además de inhibir competitivamente el acople de andrógenos al receptor, dificulta la traslocación nuclear de los receptores androgénicos. No presenta actividad androgénica. Su metabolito principal activo es N-desmetil enzalutamida y presenta actividad in vitro similar a la Enzalutamida.
La actividad de Enzalutamida permanece inclusive en casos de sobreexpresión de receptores androgénicos y de células prostáticas cancerosas con resistencia a los antiandrógenos. Enzalutamida disminuye el crecimiento de estas células, pudiendo inducir su muerte con la consiguiente reducción del volumen tumoral.
Farmacocinética: La farmacocinética de enzalutamida se ha evaluado en pacientes con cáncer de próstata y en hombres sanos. La vida media terminal (t½) de Enzalutamida en pacientes que han recibido una dosis oral única de cápsulas blandas, es de 5.8 días (intervalo de 2.8 a 10.2 días), y el estado estacionario se alcanza en aproximadamente un mes. Con la administración diaria por vía oral, Enzalutamida se acumula aproximadamente 8.3 veces más que una dosis única. Las fluctuaciones diarias de las concentraciones plasmáticas son bajas (cociente entre concentración mínima y máxima de 1.25). El aclaramiento de Enzalutamida se realiza principalmente, por metabolismo hepático, produciendo un metabolito activo que es igual de activo que Enzalutamida y que circula aproximadamente en la misma concentración plasmática que Enzalutamida.
Absorción: Estudios en humanos realizados con Enzalutamida encontraron que su absorción oral es de al menos 84%, llegando a su concentración plasmática máxima (Cmáx) entre 1 y 2 horas después de la administración. Los valores medios de Cmáx para Enzalutamida son de 16.6 μg/mL y de 12.7 μg/mL para su metabolito activo. Los alimentos carecen de efecto clínicamente significativo sobre el grado de absorción. En los ensayos clínicos, Enzalutamida se administró sin tener en cuenta la ingesta de alimentos.
Distribución: Estudios realizados cono monodosis oral estimaron un volumen de distribución de 110 L, lo que indica amplia distribución extravascular. Estudios en roedores mostraron que atraviesa la barrera hematoencefálica. Enzalutamida se une a las proteínas plasmáticas en un 97 a 98%, principalmente a la albúmina. El metabolito activo se une a las proteínas plasmáticas en un 95%. No hubo desplazamiento de la unión a proteínas entre Enzalutamida y otros fármacos de alta unión (warfarina, ibuprofeno y ácido salicílico) in vitro.
Metabolismo y Eliminación: Enzalutamida se metaboliza por las enzimas CYP2C8 y, en menor grado, por el CYP3A4/5, transformándose en dos metabolitos principales, uno activo, la N-desmetil-enzalutamida y el segundo, inactivo, es un derivado del ácido carboxílico.
En condiciones de uso clínico, Enzalutamida es un inductor potente del CYP3A4, un inductor moderado del CYP2C9 y CYP2C19, y carece de efectos clínicamente significativos sobre el CYP2C8.
El aclaramiento medio (CL/F) de Enzalutamida en pacientes oscila entre 0.520 y 0.564 L/h. Después de la administración oral de 14C-Enzalutamida, el 84.6% de la radiactividad se recupera 77 días después de la administración: el 71.0% se recupera en la orina (principalmente en forma de metabolito inactivo, con cantidades mínimas de Enzalutamida y del metabolito activo) y el 13.6% en las heces (0.39% de la dosis en forma de Enzalutamida sin modificar).
Farmacocinética en poblaciones específicas:
Insuficiencia Renal: No se han realizado estudios clínicos con Enzalutamida en pacientes con insuficiencia renal con creatininemias superiores a 2 mg/dL, ni en insuficiencia renal grave, por lo que se aconseja precaución en el tratamiento de estos pacientes. Es poco probable que la diálisis peritoneal o bien hemodiálisis intermitentes puedan eliminar la Enzalutamida en forma significativa.
Insuficiencia Hepática: Se han realizado estudios clínicos con Enzalutamida en pacientes con insuficiencia hepática leve, moderada o grave (clases A, B y C de Child-Pugh) comparando con controles sanos. En pacientes con insuficiencia hepática leve, moderada y grave, el AUC del metabolito activo N-desmetil- enzalutamida fue similar a la encontrada en sujetos sanos, por lo que no es necesario el ajuste en insuficiencia leve y moderada, aunque se recomienda precaución en los pacientes con insuficiencia hepática grave. Esto se debe a que otros estudios mostraron un incremento de Enzalutamida libre del 34% del AUC con un descenso del 27% del metabolito activo libre en pacientes con insuficiencia hepática grave.
Género: El uso de Enzalutamida no se encuentra indicado en mujeres. No se realizaron estudios en mujeres.
Raza: Los estudios clínicos de Enzalutamida realizados en pacientes con cáncer de próstata, caucásicos y japoneses demostraron datos farmacocinéticos equivalentes. No se realizaron estudios en otras razas.
Personas de edad avanzada: No se observó un efecto clínicamente relevante de la edad sobre la farmacocinética de Enzalutamida en el análisis de farmacocinética poblacional.
Efectos de la alimentación en la absorción oral: Los alimentos no tienen efectos clínicamente significativos sobre el grado de exposición a Enzalutamida. En los ensayos clínicos, Enzalutamida se ha administrado sin tener en cuenta la ingesta de alimentos.
HALLAZGOS DE LABORATORIO CLÍNICO:
Hallazgos de Laboratorio: En los estudios de eficacia y seguridad se observó una asociación entre Enzalutamida y reducción en los recuentos de leucocitos y neutrófilos. Esto no se vio asociado a manifestaciones clínicas de importancia .
Durante el tratamiento con Enzalutamida no se observaron cambios clínicamente significativos respecto a los valores basales o al grupo placebo en las pruebas de función hepática ni de función renal (nitrógeno ureico, creatinina, potasio). Tampoco se observaron cambios relevantes en los niveles de hemoglobina, plaquetas, cloruros, sodio, magnesio, fosfato, calcio ni creatinquinasa.
Se observó hiperglucemia leve en 73% del grupo tratado con Enzalutamida respecto a 60% en el grupo placebo. No hubo diferencias significativas entre grupos con hiperglucemias moderadas (4% vs 3%) con tendencia inversa en las hiperglucemias graves (2.9% vs 3.6%).
Cuando Enzalutamida se asoció a tratamiento quimioterápico, se registraron descensos en los niveles de LDH y fosfatasa alcalina a lo largo del tiempo, comparados con los valores basales y los del grupo placebo.
CONTRAINDICACIONES:
ZALUTEX se encuentra contraindicado en pacientes con hipersensibilidad al principio activo (Enzalutamida) o cualquiera de los componentes de su formulación.
Está contraindicado su uso en mujeres embarazadas o que puedan quedar embarazadas. El uso de Enzalutamida está contraindicado en menores de 18 años de edad.
RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA:
Fertilidad, Embarazo y Lactancia:
Fertilidad: estudios realizados en ratas y perros machos demostraron que Enzalutamida afecta el sistema reproductor.
Teniendo en cuenta los estudios de toxicidad en animales, Enzalutamida puede perjudicar la fertilidad de los pacientes varones con capacidad reproductiva.
Mujeres en edad fértil: no hay datos relativos al uso de Enzalutamida en mujeres embarazadas por tanto este medicamento no debe utilizarse en mujeres en edad fértil. Este medicamento puede ser perjudicial para el feto o puede provocar un aborto si lo toma una mujer embarazada.
Anticoncepción en hombres y mujeres: se desconoce si Enzalutamida y/o sus metabolitos se encuentran presentes en el semen. Debido a los hallazgos de daño embriofetal y pérdida de embarazos obtenidos en los estudios pre-clínicos de toxicidad embriofetal en animales, se debe asesorar a los pacientes varones que tengan parejas sexuales femeninas con capacidad reproductivas que utilicen métodos anticonceptivos eficaces durante el tratamiento con Enzalutamida y durante los tres meses posteriores a la última toma del medicamento.
Embarazo: ZALUTEX se encuentra contraindicado en el embarazo ya que puede causar daño embriofetal y pérdida del embarazo. ZALUTEX no tiene indicación en mujeres.
Lactancia: ZALUTEX no se encuentra indicado para su uso en mujeres. No se dispone de datos sobre la presencia de Enzalutamida y/o sus metabolitos en leche humana, ni de los efectos del fármaco en el lactante alimentado con leche materna ni del efecto del fármaco sobre la producción de leche. En estudios pre-clínicos en ratas se encontró presencia de Enzalutamida y/o sus metabolitos en la leche de rata en período de lactancia.
EFECTO EN LA CAPACIDAD PARA CONDUCIR Y UTILIZAR MÁQUINAS:
Efectos sobre la capacidad de Manejar vehículos y maquinarias: Debido a que se han notificado eventos neurológicos y psiquiátricos, incluyendo convulsiones, se debe advertir a los pacientes sobre el riesgo de manejar vehículos o maquinarias, donde la pérdida repentina del conocimiento puede causar daño grave a ellos mismos como a terceras personas.
PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD:
Carcinogénesis, mutagénesis y fototoxicidad: No se han llevado a cabo estudios a largo plazo en animales para la evaluación de la posibles acción cancerígena de Enzalutamida.
En el ensayo de mutagénesis microbiana (Ames) Enzalutamida no indujo mutaciones. Enzalutamida resultó no clastogénica tanto en el ensayo citogenético in vitro con células de linfoma de ratón como en el ensayo in vivo de micronúcleos de ratón.
Enzalutamida resultó ser no fototóxica en estudios in vitro.
REACCIONES ADVERSAS:
Las reacciones adversas más frecuentes son astenia/fatiga, sofocos, fracturas e hipertensión. Otras reacciones adversas importantes incluyen caídas, trastornos cognitivos y neutropenia.
Las crisis epilépticas se presentaron en el 0.4% de los pacientes tratados con Enzalutamida, el 0.1% de los pacientes tratados con placebo y el 0.3% de los pacientes tratados con bicalutamida.
Se han notificado casos raros de síndrome de encefalopatía posterior reversible en pacientes tratados con Enzalutamida (ver sección advertencias).
Se ha notificado síndrome de Stevens-Johnson asociado al tratamiento con enzalutamida (ver sección advertencias).
En ensayos clínicos publicados aleatorizados y controlados con placebo, el 2.5% de los pacientes tratados con Enzalutamida más terapia de deprivación de andrógenos (TDA) presentaron cardiopatía isquémica, frente al 1.3% de los pacientes tratados con placebo más TDA.
La frecuencia de reacciones adversas se ordena de acuerdo a la siguiente clasificación:
- Muy Frecuentes (>1/10)
- Frecuentes (>1/100 a < 1/10)
- Poco Frecuentes (>1/1000 a < 1/100)
- Raras (>1/10000 a < 1/1000)
- Muy Raras (<1/10000)
Frecuencia no conocida (no puede estimarse a partir de los datos disponibles)
Las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo de frecuencia.
Reacciones Adversas Identificadas en ensayos clínicos controlados y post-comercialización
|
Clasificación de Órganos según MedDRA |
Frecuencia |
|---|---|
|
Trastornos de la Sangre y del Sistema Linfático |
Poco Frecuentes: leucopenia, neutropenia No conocida*: trombocitopenia |
|
Trastornos del Sistema inmunológico |
No conocida*: edema de cara, edema de lengua, edema de labio y edema faríngeo. |
|
Trastornos generales |
Muy Frecuentes: astenia/fatiga. |
|
Trastornos psiquiátricos |
Frecuentes: ansiedad. Poco Frecuentes: alucinaciones visuales |
|
Trastornos del Sistema nervioso |
Muy Frecuentes: cefalea Frecuentes: alteración de la memoria, amnesia, alteración de la atención, síndrome de piernas inquietas. Poco Frecuentes: trastorno cognitivo, crisis epiléptica. No conocida*: síndrome de encefalopatía posterior reversible. |
|
Trastornos cardíacos |
Frecuentes: cardiopatía isquémica No conocida*: prolongación del intervalo QT |
|
Trastornos del aparato reproductor y de la mama |
Frecuentes: ginecomastia |
|
Trastornos vasculares |
Muy Frecuentes: sofocos, hipertensión |
|
Trastornos gastrointestinales |
No conocida*: náuseas, vómitos, diarrea |
|
Trastornos hepatobiliares |
Poco frecuentes: enzimas hepáticas elevadas |
|
Trastornos de la piel y del tejido subcutáneo |
Frecuentes: piel seca, prurito No conocida*: erupción, eritema multiforme, síndrome de Stevens-Johnson. |
|
Trastornos musculoesqueléticos y del tejido conectivo |
Frecuentes: fracturas** No conocida*: mialgia, espasmos musculares, debilidad muscular, dolor de espalda. |
|
Otros |
Frecuentes: caídas |
* Notificaciones espontáneas procedentes de la experiencia post-comercialización
** Incluyen todas las fracturas, excepto las fracturas patológicas.
Experiencia post comercialización: Durante el uso posterior a la aprobación de Enzalutamida se notificaron las siguientes reacciones adversas. Debido a que estas reacciones fueron notificadas en forma voluntaria sobre una población de tamaño no conocido se carece de estadísticas para determinar en forma confiable la frecuencia del evento y la relación de causalidad con la exposición a Enzalutamida.
- En todo el cuerpo: hipersensibilidad (edema de lengua, de labios y de faringe).
- Trastornos gastrointestinales: vómitos.
- Trastornos neurológicos: síndrome de encefalopatía posterior reversible (SERP).
- Trastornos del tejido subcutáneo: erupción.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO:
Interacción con otros fármacos:
• Posibilidad de que otros medicamentos modifiquen la exposición a Enzalutamida
Inhibidores del CYP2C8: el CYP2C8 cumple un rol importante en la eliminación de Enzalutamida y en la formación de su metabolito activo. Después de la administración oral a hombres sanos de gemfibrozil (600 mg dos veces al día), un inhibidor potente de CYP2C8, el AUC de Enzalutamida aumentó un 326%, mientras que la Cmáx de Enzalutamida disminuyó un 18%. Para la suma de Enzalutamida libre más el metabolito activo libre, el AUC aumentó un 77%, mientras que la Cmáx disminuyó un 19%. Se recomienda evitar o usar con precaución los inhibidores potentes de CYP2C8 (por ejemplo gemfibrozil) durante el tratamiento con Enzalutamida. Si se debe administrar simultáneamente a los pacientes un inhibidor potente del CYP2C8, la dosis de Enzalutamida se debe reducir a 80 mg una vez al día.
Inhibidores del CYP3A4: en el metabolismo de Enzalutamida el CYP3A4 desempeña un papel secundario. Después de la administración oral a hombres sanos de un inhibidor potente del CYP3A4 como itraconazol (200 mg una vez al día), el AUC de Enzalutamida se incrementó un 41%, mientras que la Cmáx se mantuvo. Para la suma de Enzalutamida libre más el metabolito activo libre, el AUC aumentó un 27%, mientras que la Cmáx se mantuvo nuevamente. No es necesario ajustar la dosis al administrar Enzalutamida simultáneamente con inhibidores del CYP3A4.
Inductores del CYP2C8 y CYP3A4: se efectuaron estudios en voluntarios sanos de sexo masculino, a los que se les administró rifampicina 600 mg por día. Éste es un inductor moderado del CYP2C8 y un inductor potente del CYP3A4. La administración posterior de Enzalutamida mostró un descenso del 37% del AUC de Enzalutamida y su metabolito activo, sin variaciones en la Cmáx. Por ello no es necesario ajustar la dosis de Enzalutamida cuando se administra con inductores del CYP2C8 o CYP3A4.
Sin embargo se sugiere evitar el uso concomitante de inductores con índice terapéutico estrecho (ej: alfentanilo, ciclosporina, ergotamina, dihidroergotamina, fentanilo, pimozida, quinidina, sirolimus y tacrolimus).
Carbamazepina, fenobarbital, fenitoína, rifabutina, rifampicina, rifapentina y hierba de San Juan pueden disminuir el nivel plasmático de Enzalutamida pudiendo requerir un aumento de dosis de ésta, si no puede evitarse el uso concomitante de estos inductores enzimáticos.
• Posibilidad de que Enzalutamida modifique la exposición a otros medicamentos
A su vez, y dado que Enzalutamida es un inductor enzimático potente (CYP3A4 de hígado e intestino, CYP2B6, CYP 2C9, CYP2C19), pudiendo también inducir a la uridina difosfo-glucuroniltransferasa (UGT, enzimas de conjugación glucurónica) y proteínas transportadoras como gp-P, pudiendo afectar la eficacia de otros medicamentos. Esto podría incluir también a la proteína asociada a resistencia a múltiples drogas (MRP2) y la proteína de resistencia al cáncer de mama (BCRP) y el polipéptido transportador de aniones orgánicos 1B1 (OATP1B1). Antes de iniciar el tratamiento con Enzalutamida se debe realizar una revisión de toda la medicación concomitante.
Estudios publicados han demostrado que Enzalutamida es inductor potente de CYP3A4 e inductor moderado de CYP2C9 y CYP2C19. En pacientes con cáncer de próstata, la administración simultánea de Enzalutamida (160 mg al día) con dosis orales únicas de sustratos sensibles del CYP como midazolam, warfarina u omeprazol, provocó una disminución del 86% del AUC de midazolam; 56% del AUC de warfarina y 70% de omeprazol. Otro estudio publicado no mostró un efecto importante sobre la farmacocinética de docetaxel administrado por vía intravenosa (el AUC disminuyó 12% y la Cmáx 4%).
Por ello se debe evitar el uso concomitante con warfarina y anticumarínicos. En caso de utilizarse, se deberán efectuar controles adicionales de la coagulación mediante la razón internacional normalizada (RIN).
Se esperan interacciones con determinados medicamentos que se eliminan a través del metabolismo de transporte activo. Se recomienda evitar o usar con precaución estos medicamentos si su efecto terapéutico es de gran importancia para el paciente, y no se pueden realizar fácilmente ajustes de dosis basados en un seguimiento de la eficacia o de las concentraciones plasmáticas. Se sospecha que el riesgo de lesión hepática después de la administración de paracetamol es mayor en pacientes tratados concomitantemente con inductores enzimáticos.
Los siguientes grupos de medicamentos pueden ser afectados por el uso concomitante con Enzalutamida:
- Analgésicos (por ejemplo: tramadol, fentanilo)
- Antibióticos (por ejemplo: claritromicina, doxiciclina)
- Agentes utilizados en oncología (por ejemplo: cabazitaxel)
- Anticoagulantes (por ejemplo: acenocumarol, warfarina)
- Antiepilépticos (por ejemplo: carbamazepina, clonazepam, fenitoína, primidona, ácido valproico)
- Antipsicóticos (por ejemplo: haloperidol)
- Betabloqueantes (por ejemplo: bisoprolol, propranolol)
- Bloqueantes de canales de calcio (por ejemplo: diltiazem, felodipina, nicardipina, nifedipina, verapamilo)
- Glucósidos cardíacos (por ejemplo: digoxina)
- Corticoides (por ejemplo: dexametasona, prednisolona)
- Antivirales anti VIH (por ejemplo: indinavir, ritonavir)
- Hipnóticos (por ejemplo: diazepam, midazolam, zolpidem)
- Enzimas metabolizadas por CYP3A4 (por ejemplo: atorvastatina, simvastatina)
- Medicamentos tiroideos (por ejemplo: levotiroxina)
Las acciones de Enzalutamida que afecten los niveles plasmáticos de otros medicamentos podrían observarse al cabo de un mes de tratamiento, cuando se llega al nivel estacionario, o previamente a alcanzar este nivel. Dada la semivida prolongada de Enzalutamida (5.8 días), estos efectos pueden persistir un mes o más después de la interrupción de Enzalutamida. Tras su interrupción podría ser necesaria una reducción gradual de la dosis del medicamento concomitante.
Sustratos del CYP1A2 y CYP2C8: Enzalutamida (160 mg una vez al día) no provocó una variación clínicamente significativa del AUC o de la Cmáx de cafeína (sustrato del CYP1A2) o pioglitazona (sustrato del CYP2C8). El AUC de pioglitazona aumentó un 20% mientras que la Cmáx disminuyó en un 18%. El AUC y la Cmax de cafeína disminuyeron un 11% y un 4% respectivamente. No se sugiere realizar ajuste de la dosis al administrar un sustrato del CYP1A2 o CYP2C8 simultáneamente con Enzalutamida.
Sustratos de la gp-P: cuando se utilizan concomitantemente medicamentos sustratos de la gp-P (por ejemplo colchicina, dabigatrán o digoxina), estos se deben usar con precaución y pueden requerir un ajuste de dosis.
El uso concomitante de Enzalutamida con omeprazol provocó una disminución en los niveles plasmáticos de omeprazol.
Sustratos de BCRP, MRP2, OAT3 y OCT1: según los datos obtenidos in vitro, no se puede descartar la inhibición de la BCRP y MRP2 (en el intestino), así como la del transportador de aniones orgánicos 3 (OAT3) y la del transportador de cationes orgánicos 1 (OCT1) (sistémicamente). Teóricamente la inducción de estos transportadores también es posible, y actualmente el efecto neto se desconoce.
Medicamentos que producen una prolongación del intervalo QT: debido a que el tratamiento de deprivación androgénica puede producir una prolongación del intervalo QT, el uso concomitante de Enzalutamida con medicamentos que producen una prolongación del intervalo QT o de medicamentos capaces de inducir Torsades de pointes, tales como antiarrítmicos de clase IA (por ejemplo: quinidina, disopiramida) o de clase III (por ejemplo: amiodarona, sotalol, dofetilida, ibutilida), metadona, moxifloxacino, antipsicóticos, etc., deben ser cuidadosamente evaluados.
PRECAUCIONES Y ADVERTENCIAS:
Advertencias:
Reacciones cutáneas graves: Se han notificado reacciones adversas cutáneas graves (RACG) asociadas al tratamiento con enzalutamida, incluido el síndrome de Stevens Johnson, que pueden poner en peligro la vida o ser mortales.
En el momento de la prescripción, se debe informar a los pacientes de los signos y síntomas y vigilarles estrechamente por si aparecen reacciones cutáneas.
Si aparecen signos o síntomas indicativos de esta reacción, se debe suspender de inmediato enzalutamida y considerar un tratamiento alternativo adecuado.
Riesgo de Convulsiones: En pacientes que hayan padecido convulsiones o con factores predisponentes como lesiones cerebrales, accidente cerebrovascular, tumores cerebrales primarios o metastásicos o alcoholismo, se debe tener precaución en el uso de Enzalutamida. Asimismo, el riesgo de convulsiones puede ser mayor en pacientes que consuman medicamentos que desciendan el umbral epiléptico.
En caso de que los pacientes sufrieran crisis epilépticas, la decisión de continuar o no el tratamiento deberá evaluarse de acuerdo al caso clínico.
Síndrome de encefalopatía posterior reversible (SEPR): El SEPR es un trastorno del sistema nervioso central que se ha notificado con frecuencia rara y reversible, en pacientes que recibían Enzalutamida. El SEPR puede evolucionar rápidamente, con sintomatología consistente en cefalea, alteraciones visuales, confusión y convulsiones, pudiendo presentar asimismo hipertensión arterial. El diagnóstico se SEPR deberá confirmarse mediante estudios de imagen cerebral como resonancia magnética. En estos casos se recomienda interrumpir el tratamiento con Enzalutamida.
Uso concomitante con cumarínicos: Se recomienda no administrar en forma concomitante Enzalutamida con warfarina u otros anticoagulantes cumarínicos (metabolizados por el CYP2C9). En caso de ser necesaria la coadministración deben realizarse determinaciones periódicas de la Razón Internacional Normalizada (RIN).
Precauciones:
Insuficiencia Renal: No se ha estudiado la seguridad de Enzalutamida en pacientes con insuficiencia renal grave, por lo que en caso de administrarse requiere precaución.
Insuficiencia hepática grave: No se conoce la importancia clínica del aumento de la vida media de Enzalutamida en pacientes con insuficiencia hepática grave. El tiempo necesario para llegar al nivel plasmático estable puede aumentar, así como el tiempo de eliminación y de sus efectos enzimáticos.
Enfermedad cardiovascular reciente: No se realizaron estudios incluyendo pacientes con infarto de miocardio ocurrido con menos de 6 meses de antelación, o en pacientes con angina inestable durante los últimos 3 meses. No fueron incluidos pacientes con fracción de eyección ventricular izquierda menor del 45%, ni pacientes con bradicardia o hipertensión no controlada. Esto debe tenerse en cuenta en el caso de prescribir Enzalutamida.
Hipertensión arterial: En estudios clínicos publicados aleatorizados controlados con placebo se informaron casos de hipertensión en un 11% de los pacientes que recibieron Enzalutamida, y en un 4% de los pacientes que recibieron placebo. Ninguno de los pacientes sufrió una crisis hipertensiva. Los antecedentes de hipertensión fueron parejos para ambos grupos. La discontinuación del estudio debida al evento hipertensivo fue < 1% de los pacientes de cada grupo. Se desconoce si existe una relación causal entre Enzalutamida e hipertensión. No se asoció la administración de Enzalutamida a hipocalcemia ni a exceso de mineralocorticoides como retención hídrica. Los casos observados de hipertensión arterial en los pacientes que recibían Enzalutamida fueron tratados exitosamente con las medidas antihipertensivas estándar.
Prolongación del Intervalo QT: Se ha observado un alargamiento del intervalo QT durante el tratamiento con deprivación androgénica. El uso de medicación concomitante que prolongue el intervalo QT podría aumentar este riesgo, incluyendo el de Torsade de pointes, los que debe ser evaluado por el médico antes de comenzar el tratamiento con Enzalutamida. Ejemplo de este tipo de medicamentos son los antiarrítmicos de Clase IA (por ejemplo: quinidina, disopiramida), de clase III (por ejemplo: amiodarona, sotalol, dofetilida, ibutilida), metadona, moxifloxacino, antipsicóticos, etc.
Uso concomitante con otros medicamentos: Enzalutamida es un inductor enzimático potente y puede dar lugar a una pérdida de eficacia de muchos medicamentos de uso común. Cuando se inicia el tratamiento con Enzalutamida se debe realizar una revisión de los medicamentos concomitantes. Generalmente se debe evitar el uso concomitante con medicamentos sustratos sensibles de enzimas o transportadores metabólicos.
Uso con quimioterapia: Se desconoce si el uso concomitante de Enzalutamida con quimioterapia citotóxica tiene un efecto sobre la eficacia y seguridad del mismo. Si bien no se observó un efecto significativo sobre la farmacocinética de docetaxel, la administración simultánea podría incrementar el riesgo de neutropenia inducida por docetaxel.
Caídas/fracturas no patológicas: En dos estudios clínicos publicados aleatorizados, controlados con placebo se produjeron caídas (o lesiones relacionadas con caídas) en un 9% de los pacientes tratados con Enzalutamida y en un 4% en los pacientes tratados con placebo. Las caídas no estaban relacionadas con pérdida de conocimiento ni con convulsiones. Las lesiones por caídas fueron más graves en el grupo de pacientes tratados con Enzalutamida y consistieron en fracturas no patológicas, lesiones articulares y hematomas.
Las caídas en el grupo tratado con Enzalutamida ocurrieron en su mayoría dentro de los primeros 6 meses de tratamiento. En ambos grupos (Enzalutamida y placebo) la frecuencia de caídas aumentó con la edad de los pacientes. Si bien se desconoce el factor causal común de las caídas, las mismas se atribuyeron a diversos factores, como debilidad por privación de andrógenos o el uso concomitante de otros medicamentos. La mayoría de las caídas fueron catalogadas como accidentales o mecánicas y coincidieron con una tendencia al aumento de las fracturas no patológicas que se informaron después de 6 meses de tratamiento. Aproximadamente 50% de los pacientes con fracturas no patológicas habían sufrido una caída durante los 14 días anteriores. A su vez, las caídas y fracturas no patológicas asociadas fueron algo más frecuentes con los mayores tiempos de exposición al tratamiento.
Reacciones de hipersensibilidad: Se han observado reacciones de hipersensibilidad con el tratamiento con Enzalutamida (ver sección REACCIONES ADVERSAS), que se manifiestan por síntomas que incluyen, aunque no exclusivamente, edema de lengua, edema de labio y edema faríngeo.
Se han notificado reacciones adversas cutáneas graves (RACG) con enzalutamida. En el momento de la prescripción, se debe informar a los pacientes de los signos y síntomas y vigilarles estrechamente por si aparecen reacciones cutáneas.
Cápsula deshumidificadora: El envase contiene una cápsula deshumidificadora la cual no debe ingerirse, tragarse ni masticarse.
Contiene Lactosa: Pacientes con problemas hereditarios raros de intolerancia a galactosa, deficiencia de lactasa de Lapp o con mala absorción de glucosa o galactosa no deben tomar este medicamento.
DOSIS Y VÍA DE ADMINISTRACIÓN:
Dosis y administracion: La dosis recomendada es de 160 mg (cuatro cápsulas de 40 mg) en una sola dosis diaria por vía oral.
El medicamento no debe partirse ni masticarse.
En los pacientes que no fueron sometidos a castración quirúrgica se debe mantener la castración hormonal con un análogo de LHRH durante el tratamiento con ZALUTEX.
Si un paciente olvidó tomar la dosis prescripta en su horario habitual, deberá tomar la dosis prescripta lo más cerca posible del horario habitual.
Si un paciente olvidó tomar la dosis durante un día entero debe reanudar al día siguiente el tratamiento tomado la dosis diaria habitual.
Si un paciente presenta toxicidad de Grado ≥ 3 o una reacción adversa intolerable, se debe suspender la administración durante una semana o hasta que los síntomas mejoren a Grado ≤ 2, y posteriormente restablecer la misma dosis o una dosis reducida (120 mg u 80 mg) siempre que esté justificado.
Uso concomitante con inhibidores potentes del CYP2C8: Dado que el CYP2C8 es importante para la metabolización de Enzalutamida, en lo posible debe evitarse el uso de inhibidores potentes del CYP2C8 cuando se está administrando Enzalutamida.
Cuando se administró gemfibrozil 600 mg dos veces por día se observó un incremento del AUC de Enzalutamida de 326%. En el caso de ser co-administrados, se recomienda reducir la dosis de Enzalutamida a 80 mg por día, volviendo a las dosis anteriores una vez suspendida la administración de los inhibidores de CYP2C8.
Uso en poblaciones especiales:
Personas de edad avanzada: No es necesario ajustar la dosis en personas de edad avanzada.
Insuficiencia hepática: En pacientes con insuficiencia hepática leve o moderada (Clase A o B de Child Pugh) no es necesario ajustar la dosis. No se recomienda administrar Enzalutamida a pacientes con insuficiencia hepática grave (Clase C de Child Pugh).
Insuficiencia renal: En pacientes con insuficiencia renal leva a moderada no es necesario ajustar la dosis de Enzalutamida, recomendándose precaución en los pacientes con enfermedad renal grave.
Población pediátrica: Enzalutamida no está indicada para su uso en niños.
ZALUTEX se debe administrar por vía oral. Las cápsulas se deben tragar enteras con agua y se pueden tomar con o sin alimentos.
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL:
Sobredosificación: No existe ningún antídoto para Enzalutamida. En caso de sobredosis, se debe interrumpir el tratamiento con Enzalutamida e iniciar medidas de apoyo general teniendo en cuenta que su vida media es de 5,8 días. Tras una sobredosis, los pacientes pueden tener un mayor riesgo de sufrir convulsiones.
Ante la eventualidad de una sobredosificación, concurrir al hospital más cercano.
PRESENTACIÓN:
Bolsa con 120 cápsulas duras.
RECOMENDACIONES SOBRE ALMACENAMIENTO:
Recomendaciones en caso sobredosificacion: No existe ningún antídoto para Enzalutamida. En caso de sobredosis se debe interrumpir el tratamiento con Enzalutamida e iniciar medidas de apoyo general teniendo en cuenta que su vida media es de 5.8 días. Después de una sobredosis, los pacientes pueden tener un mayor riesgo de sufrir convulsiones.
Ante la eventualidad de una sobredosificación concurrir al hospital más cercano o comunicarse con los centros de toxicología.
Ante la eventualidad de una sobredosificación, concurrir al hospital más cercano o comunicarse con los centros de toxicología:
Abuso y adiccion: No se dispone de información acerca de abuso y adicción de Enzalutamida. Enzalutamida no tiene un potencial adictivo como la dependencia y la tolerancia, por lo que la posibilidad de uso indebido con fines ilegales es insignificante
Acción terapeutica: Tratamiento antineoplásico hormonal, terapia antineoplásica endócrina.
Código ATC: L02BB04
REFERENCIAS BIBLIOGRÁFICAS:
Scher, H. I., Fizazi, K., Saad, F., Taplin, M.-E., Sternberg, C. N., Miller, K., de Wit,
R., Mulders, P., Chi, K. N., Shore, N. D., Armstrong, A. J., Flaig, T. W., Fléchon, A., Mainwaring, P., Fleming, M., Hainsworth, J. D., Hirmand, M., Selby, B., Seely, L., & de Bono, J. S. (2012). Increased Survival with Enzalutamide in Prostate Cancer after Chemotherapy. New England Journal of Medicine, 367(13), 1187–1197. https://doi.org/10.1056/nejmoa1207506
Beer, T. M., Armstrong, A. J., Rathkopf, D. E., Loriot, Y., Sternberg, C. N., Higano,
C. S., Iversen, P., Bhattacharya, S., Carles, J., Chowdhury, S., Davis, I. D., de Bono,
J. S., Evans, C. P., Fizazi, K., Joshua, A. M., Kim, C.-S., Kimura, G., Mainwaring, P., Mansbach, H., & Miller, K. (2014). Enzalutamide in metastatic prostate cancer before chemotherapy. The New England Journal of Medicine, 371(5), 424–433. https://doi.org/10.1056/NEJMoa1405095
Shore, N. D., Chowdhury, S., Villers, A., Klotz, L., Siemens, D. R., Phung, D., Os,
S. van, Hasabou, N., Wang, F., Bhattacharya, S., & Heidenreich, A. (2016). Efficacy and safety of enzalutamide versus bicalutamide for patients with metastatic prostate cancer (TERRAIN): a randomised, double-blind, phase 2 study. The Lancet Oncology, 17(2), 153–163. https://doi.org/10.1016/S1470-2045(15)00518-5
Hussain, M., Fizazi, K., Saad, F., Rathenborg, P., Shore, N., Ferreira, U., Ivashchenko, P., Demirhan, E., Modelska, K., Phung, D., Krivoshik, A., & Sternberg, C. N. (2018). Enzalutamide in Men with Nonmetastatic, Castration-
Resistant Prostate Cancer. New England Journal of Medicine, 378(26), 2465–2474. https://doi.org/10.1056/nejmoa1800536
Sternberg, C. N., Fizazi, K., Saad, F., Shore, N. D., De Giorgi, U., Penson, D. F., Ferreira, U., Efstathiou, E., Madziarska, K., Kolinsky, M. P., Cubero, D. I. G., Noerby, B., Zohren, F., Lin, X., Modelska, K., Sugg, J., Steinberg, J., & Hussain, M. (2020). Enzalutamide and Survival in Nonmetastatic, Castration-Resistant Prostate Cancer. New England Journal of Medicine, 382(23), 2197–2206. https://doi.org/10.1056/nejmoa2003892
Xtandi 40 mg cápsulas. Astellas Pharma Europe B.V. Sylviusweg 62 2333 BE Leiden Países Bajos. https://cima.aemps.es/cima/pdfs/es/p/113846002/P_113846002.pdf.
Modificaciones de la información de los medicamentos autorizados por procedimiento nacional que contienen: Enzalutamida. https://cima.aemps.es/cima/psusa.do?metodo=verDoc&id=3281
Berkanafarma S.A.
